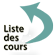Les deux éléments parasitaires visibles sont situés à l’apex de l’entérocyte. À gauche, on distingue les microvillosités de la bordure en brosse entourant le parasite. À droite, un schizonte : la coupe intéresse plusieurs mérozoïtes de C. parvum.
Introduction
En dehors de l’amœbose et de la giardiose, trois autres protozooses intestinales dues à des coccidies : la cryptosporidiose,la cystoisosporose et la cyclosporose, ont une importance médicale notable, que ce soit par leur fréquence, leur implication dans des épidémies d’origine alimentaire ou hydrique, ou leur caractère opportuniste chez les malades immunodéprimés. Les microsporidies, maintenant classées dans le règne fongique, et dont certaines sont responsables de troubles intestinaux, sont également traitées dans ce chapitre. Leur identification nécessite la mise en œuvre de techniques spécifiques qui ne sont pas pratiquées en routine dans tous les laboratoires.
1.1 - Épidémiologie
La cryptosporidiose est une infection causée par un protozoaire, une coccidie du genre Cryptosporidium. Il existe plusieurs espèces, dont les principales sont Cryptosporidium hominis, infectant uniquement l’Homme, et C. parvum, parasite de l’Homme et de plusieurs autres espèces de mammifères (bovins, ovins). D’autres espèces sont observées de façon beaucoup plus exceptionnelle (C. bovis, C. felis, C. muris, C. meleagridis) ; comme C. parvum, elles entraînent des troubles plus graves.
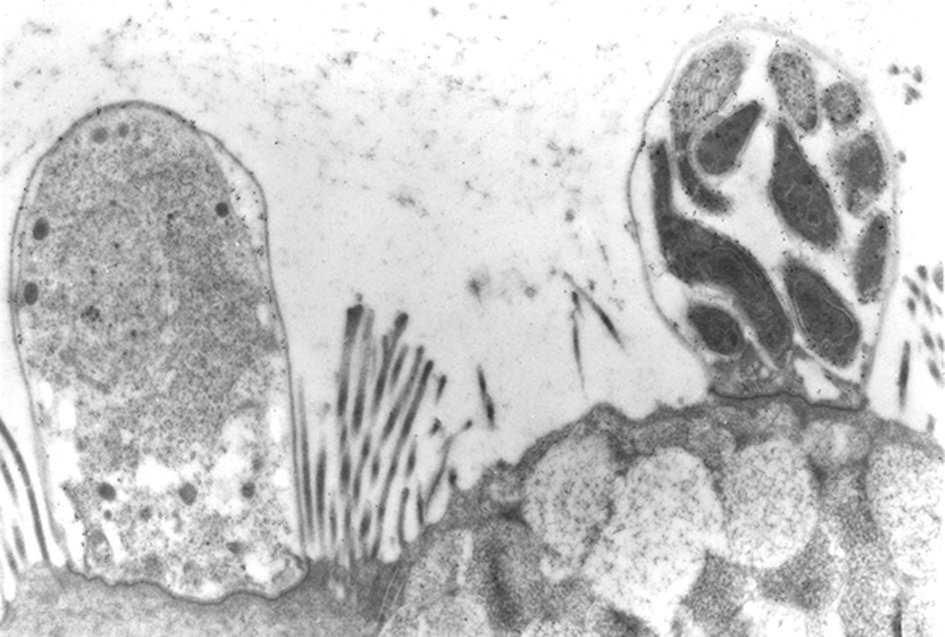
Cryptosporidium est un parasite de l’épithélium intestinal du grêle dont le cycle comporte une multiplication asexuée (schizogonie) et une multiplication sexuée (gamogonie). Ce cycle s’effectue dans une vacuole intracellulaire (vacuole parasitophore) située au niveau du pôle apical des entérocytes, juste sous la membrane, et faisant à mesure du développement du parasite protrusion dans la lumière intestinale (figure 3.1). La schizogonie conduit à la production d’un schizonte multinucléé par division binaire des noyaux et aboutit à la libération, par destruction de la cellule hôte, de mérozoïtes qui infectent d’autres cellules intestinales et assurent la dissémination parasitaire le long du tractus digestif. La production de cellules différenciées mâles et femelles (gamétocytes) initie la gamogonie avec formation des oocystes, éléments de la dissémination du parasite, qui sont éliminés avec les selles (figure 3.2). Deux types d’oocystes sont produits (paroi mince et paroi épaisse) ; ceux à paroi mince sont impliqués dans le phénomène d’auto-infestation.
Les deux éléments parasitaires visibles sont situés à l’apex de l’entérocyte. À gauche, on distingue les microvillosités de la bordure en brosse entourant le parasite. À droite, un schizonte : la coupe intéresse plusieurs mérozoïtes de C. parvum.
La contamination s’effectue par ingestion d’oocystes. Les oocystes étant directement infectants dès leur émission et très résistants dans l’environnement, la contamination peut être :
- directe entre un hôte infecté et un hôte sain : ceci explique les cas d’infections liées aux soins ; un cycle endogène (autoinfestation) est possible, favorisé par une immunodépression ;
- ou indirecte par ingestion d’eau ou d’aliments souillés par des oocystes ; l’infection peut aussi découler de la pratique d’activités aquatiques comme la baignade.
Les animaux domestiques (bovins, ovins) jouent un rôle important dans la contamination de l’environnement. L’irrigation par aspersion des cultures végétales par des eaux usées est une source de contamination des cultures. La cryptosporidiose est une parasitose cosmopolite, observée sous forme sporadique ou épidémique (réservoir d’eau de consommation, piscines, interhumaine directe, crèche, animaux infectés…), avec une incidence et une prévalence cependant très variables. Chez l’immunocompétent, en Amérique du Nord et en Europe, la cryptosporidiose est responsable de 0,6 à 2 % (7 % chez les enfants) des cas de diarrhée, alors que dans les pays en développement, elle se situe entre 4 et 32 %. On observe une variation saisonnière des cas, avec un nombre de cas plus élevé à la fin de l’été et en automne. Des taux plus élevés ont été observés chez des sujets immunodéprimés notamment atteints du sida et présentant une diarrhée chronique, de 14 % dans les pays industrialisés jusqu’à 60 % en Afrique et en Haïti. Cependant, depuis quelques années, on observe une forte diminution du nombre de cas de cryptosporidiose chez les patients infectés par le VIH grâce à la restauration immunitaire induite par les traitements antirétroviraux. Actuellement, ce sont chez des patients atteints d’autres causes d’immunodépression que sont retrouvés majoritairement les cas de cryptosporidioses : transplantés rénaux (20 % des cas), greffe de cellules souches hématopoïétiques, hémopathies…
De nombreuses épidémies sont régulièrement observées dans les pays industrialisés dues à une contamination fécale des réseaux de distribution d’eau potable, l’efficacité du chlore seul envers le Cryptosporidium étant presque nulle. L’épidémie la plus significative est survenue à Milwaukee aux États-Unis en 1993 avec plus de 400 000 personnes infectées. En France, peu de données épidémiologiques sont disponibles, mais plusieurs épidémies liées à la contamination de l’eau par Cryptosporidium ont été rapportées.