- Pré-requis et Objectifs
-
Cours
-
Contenu
- 1 - Rappel : l’hypertension et son bilan minimum
- 2 - Politique de dépistage d’une HTA secondaire
-
3 - Les hyperminéralocorticismes primaires
- 3.1 - Pathogénie et définition
- 3.2 - Présentation, prévalence et principaux types
- 3.3 - Les conditions de l’exploration
- 3.4 - Diagnostic positif de l’HAP
- 3.5 - Les tests dynamiques
- 3.6 - L’imagerie
- 3.7 - La preuve d’une sécrétion unilatérale d’aldostérone
- 3.8 - Décision thérapeutique
- 3.9 - Les hyperminéralocorticismes familiaux
- 4 - HTA endocrines iatrogènes
- 5 - Phéochromocytomes et paragangliomes fonctionnels
- 6 - Le syndrome de Cushing
- 7 - Causes rares d’HTA endocrine
-
Version PDF

-
Contenu
- Evaluations
- Annexes
6 - Le syndrome de Cushing
Le terme syndrome de Cushing regroupe toutes les situations conduisant à une hypersécrétion de cortisol (hypercortisolisme, ou hypercorticisme) endogène. Le syndrome de Cushing est rarement révélé par une HTA. Celle-ci est présente dans la majorité des Cushing mais apparaît dans les formes classiques d’hypercorticisme secondaire dans le contexte de la dysmorphie et des troubles métaboliques, gonadiques et ostéo-musculaire de ce syndrome.
6 . 1 - Les manifestations cliniques du syndrome de Cushing
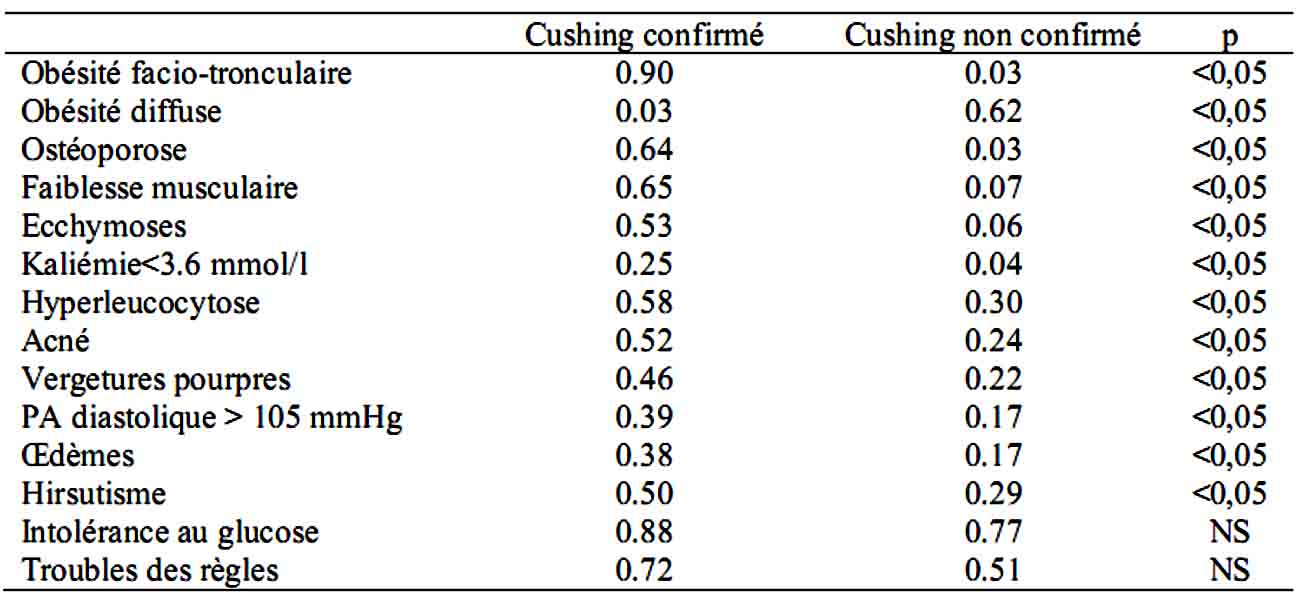
Le syndrome de Cushing sera donc recherché dans l’exploration d’une HTA lorsque les données cliniques apportent des arguments supplémentaires pour ce diagnostic. Les principales manifestations cliniques sont résumées sur le tableau 3. L’existence d’une prise de poids et d’une répartition facio-tronculaire de la masse grasse, d’une érythrose faciale et de signes d’hyper-catabolisme cutanée, osseux ou musculaire (vergetures larges et pourpres, ostéoporose, amyotrophie...) sont évocateurs. Les troubles des règles sont fréquents ainsi que l’hypogonadisme. Les troubles thymiques et l’asthénie peuvent aussi être présents. Les troubles de la tolérance glucidique et le diabète sont associés à l’hypercorticisme. L’hypokaliémie par fuite urinaire du potassium peut aussi être secondaire à l’hypersécrétion de cortisol, indépendamment d’un hyperaldostéronisme. Il est donc finalement fréquent de se trouver chez un sujet diabétique et hypertendu avec des arguments souvent peu spécifiques mais malgré tout évocateur d’hypercorticisme (érythrose faciale, prise de poids avec tendance à une répartition facio-tronculaire de la masse grasse….).
Tableau 3 : Manifestations cliniques du syndrome de Cushing Prévalence des principales caractéristiques cliniques de 211 patients explorés pour suspicion de syndrome de Cushing, pour qui le diagnostic fut finalement confirmé ou non (d’après Bertagna, et al, 1995).
6 . 2 - Etiologies du syndrome de Cushing
L’hypercorticisme peut être d’origine primitivement surrénale (syndrome de Cushing ACTH-indépendant) ou secondaire à une hypersécrétion chronique d’ACTH (syndrome de Cushing ACTH-dépendant). La cause la plus fréquente est la maladie de Cushing qui correspond à une hypersécrétion d’ACTH d’origine hypophysaire, le plus souvent par un micro-adénomeDéfinitionTumeurs mesurant moins de 10 mm corticotrope. La maladie de Cushing représente la cause de plus des deux tiers des syndromes de Cushing et est plus fréquente chez la femme (sexe ratio 2.8). La sécrétion ectopique d’ACTH par une tumeur non hypophysaire est plus rare (7 à 15% des cas de syndrome de Cushing). Il peut s’agir de tumeurs neuroendocrines différenciées bronchiques (carcinoïde, parfois difficile à localiser du fait de sa petite taille), de cancers pulmonaires à petite cellules, de tumeurs du pancréas endocrine, de tumeurs thymiques, de phéochromocytomes, de cancers médullaires de la thyroïde… Les tumeurs corticosurrénales représentent 20 à 25% des syndromes de Cushing et peuvent être bénignes (adénomes) ou malignes (cortico-surrénalomes). L’adénome sécrétant de la surrénale est responsable en règle de l’hypersécrétion d’un type unique de stéroïde : soit aldostérone (adénome de Conn entraînant l’HAP décrit plus haut), soit de cortisol (adénome responsable d’un syndrome de Cushing ACTH-indépendant). Le corticosurrénalome est souvent pluri-sécrétant : cortisol, androgènes et minéralocorticoïdes et/ou précurseurs des stéroïdes. La présentation clinique du syndrome de Cushing pourra être influencée par l’étiologie et le type de sécrétion.
6 . 3 - Les explorations hormonales du diagnostic positif du syndrome de Cushing
Les explorations biologiques sont une étape importante du diagnostic de syndrome de Cushing. Si dans des situations d’hypercortisolisme franc la confirmation de la suspicion diagnostique est souvent facile, il est parfois plus délicat d’affirmer l’hypercortisolisme dans des formes mineures ou débutantes. Le problème du diagnostique différentiel avec un hypercortisolisme modéré « fonctionnel » dans le cadre d’un « pseudo syndrome de Cushing » (dépression surtout, éthylisme, ou plus rarement anorexie…) peut alors se poser.
Explorations de base
Elles peuvent recourir à la mesure de la cortisolémie, de la cortisolurie et dans certains cas du cortisol salivaire.
La mesure de la cortisolémie évalue le cortisol total, c’est à dire la fraction libre et la fraction liée (principalement à la Corticosteroid Binding Globulin ou CBG). Le sujet normal présente un rythme nycthéméral bien connu de la cortisolémie qui est maximale le matin vers 08 h et minimale entre 24 h et 04 h du matin. La caractéristique de l’hypercortisolisme est plus une abolition de ce rythme qu’une élévation absolue de la cortisolémie. L’étude de la cortisolémie est donc surtout utile dans le cadre de prélèvements nocturnes difficilement réalisables en ambulatoire. Le cortisol salivaire a par contre dans cette situation l’avantage d’être facilement réalisable et d’offrir une grande sensibilité diagnostique. Le cortisol salivaire est un indicateur du cortisol libre plasmatique et son résultat est donc indépendant des taux de CBG. Il est utile dans le cas d’une élévation des taux de CBG (par exemple sous oestro-progestatifs) où la cortisolémie serait élevée même en l’absence d’augmentation du cortisol libre. La mesure de la cortisolurie sur 24h est l’intégration des taux de cortisol libre circulant. Sous réserve d’un recueil urinaire sur 24h correct (à bien expliquer au patient, et à vérifier par la mesure simultanée de la créatininurie) la cortisolurie a une grande sensibilité (94 à 100%) pour le diagnostic d’hypercortisolisme. Même si les études sont en faveur d’une bonne spécificité il faut se méfier des élévations modestes de la cortisolurie qui peuvent s’observer dans le cadre du pseudo-syndrome de Cushing ou lors d’un recueil incorrect des urines. A l’inverse le diagnostic de syndrome de Cushing est en général certain lorsque la cortisolurie sur 24h est régulièrement supérieure à trois fois la limite de la normale.
Explorations dynamiques
Le principe des différents tests de freinage à la dexaméthasone (DXM) est basé sur le rétrocontrôle négatif exercé physiologiquement par le cortisol sur l’axe corticotrope au niveau hypothalamo-hypophysaire. Deux tests de freinage sont classiquement utilisables pour le diagnostic positif d’hypercortisolisme : 1) le freinage minute (1 mg de dexaméthasone -DXM- à minuit, prélèvement de la cortisolémie à 8 heure le matin), 2) le freinage faible mis au point par Liddle il y a plus de 40 ans (2 mg de DXM par jour pendant 48 heures, recueil de la cortisolurie sur 24h le deuxième jour).
Le test de freinage minute à l’avantage de la simplicité et peut se réaliser en première intention en ambulatoire. Il manque cependant de spécificité et peut donner un faux positif chez les patients présentant une augmentation de la CBG (par exemple sous estrogènes) ou traités par inducteur enzymatiques augmentant le catabolisme de la DXM. Suivant les laboratoires et les centres le seuil de 18 à 40 ng/ml est utilisé pour son interprétation (un sujet sans hypercorticisme présentant après freinage une cortisolémie inférieure au seuil). Le test de freinage faible est plus lourd de réalisation mais a l’avantage d’être basé sur la mesure du cortisol libre et aurait ainsi une plus grande spécificité, le faisant très classiquement considérer comme un test de confirmation d’un freinage minute positif.
6 . 4 - Les explorations du diagnostic étiologique d’un syndrome de Cushing
Une fois le diagnostic d’hypercortisolisme formellement établi la première étape du diagnostic étiologique vise à préciser son caractère ACTH-indépendant (tumeur de la surrénale) ou au contraire ACTH-dépendant (maladie de Cushing ou sécrétion ectopique d’ACTH). Cette étape repose sur le dosage d’ACTH plasmatique qui pour être fiable doit être fait selon des conditions rigoureuses dans un laboratoire d’hormonologie. L’ACTH d’un sujet normal varie en règle entre 20 et 80 pg/ml. Un taux d’ACTH supérieur à 15 pg/ml est inadapté à l’excès de cortisol et affirme le caractère ACTH-dépendant du syndrome de Cushing. Un taux inférieur à 5 pg/ml par IRMA affirme le caractère ACTH-indépendant. Un taux entre 5 et 15 pg/ml se rencontre parfois, nécessite des explorations plus spécialisées voir des tests dynamiques (test au CRH en particulier). L’exploration d’un syndrome de Cushing ACTH-indépendant repose sur le scanner des surrénales permettant alors de visualiser la tumeur (adénome ou cancer). Le syndrome de Cushing ACTH-dépendant nécessite de recourir à des explorations biologiques plus spécialisées (principalement test fort à la DXM et test au CRH). En fonction des situations, les examens d’imageries seront centrés sur l’hypophyse (IRM) ou à la recherche d’une tumeur ectopique (TDM thoracique et/ou abdominal le plus souvent dans un premier temps). Les cas difficiles (explorations biologiques discordantes, imagerie peu ou non significative) seront explorés par dosage d’ACTH lors d’un cathétérisme des sinus pétreux en centre spécialisé.
8/9