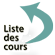Introduction
La trypanosomose humaine africaine (THA) est une maladie parasitaire endémique touchant de nombreux pays de l’Afrique Subsaharienne.
Les parasites responsables sont des protozoaires sanguicoles, Trypanosoma brucei gambiense (T. b. gambiense) en Afrique de l’Ouest et Centrale et T.b. rhodesiense en Afrique de l’Est. Ils sont transmis à l’homme par un arthropode vecteur hématophage : la glossine ou mouche Tsé-Tsé.
A l’endroit de la piqûre se développe un chancre, réaction inflammatoire locale. Il précède une infection systémique d’abord lymphatico-sanguine (phase I), puis après passage du Trypanosome dans le système nerveux central, méningo-encéphalitique (phase II).
Un des signes neurologiques fréquent est la perturbation du cycle veille-sommeil, d’où le nom de maladie du sommeil autrefois donné à la THA. En zone d’endémie, tout signe neurologique doit faire penser à l’éventualité d’une THA.
L’évolution est le plus souvent mortelle en l’absence de traitement. Celui-ci repose sur des médicaments toxiques : Pentamidine en phase I et Arsobal (un dérivé de l’arsenic en phase II). C’est dire l’intérêt d’un diagnostic précoce associé à la lutte contre les vecteurs (piégeage), réalisé par des équipes mobiles dans les foyers de THA en Afrique. L’abandon de ces programmes de lutte, les guerres, le désintérêt général, ont entraîné une recrudescence de la maladie, actuellement considérée comme une affection réémergente, posant un problème de santé publique dans quelques pays d’Afrique subsaharienne. Peu de cas importés et de voyageurs contaminés en zone d’endémie sont observés en Europe.
1 - Les parasites
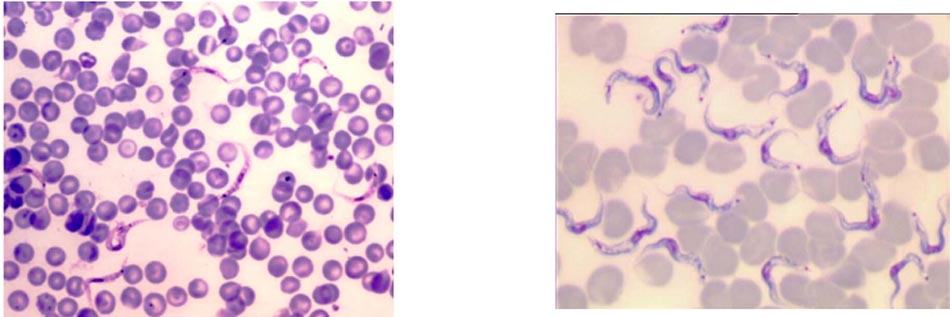
Les trypanosomes sont des protozoaires flagellés fusiformes, mis en évidence dans le sang, les ganglions, le liquide céphalo-rachidien. Ils sont très mobiles à l’état frais.
La coloration permet de visualiser un noyau central et un point postérieur à côté duquel part le flagelle (d’où son nom « kinétoplaste », alors qu’il s’agit d’ADN mitochondrial).
Le flagelle part vers l’avant, soulevant la membrane ondulante et constitue la partie antérieure du trypanosome. Leur taille varie de 12 à 42 µm de long sur 1,5 à 3,5 µm de large.
T. b. gambiense, et T. b. rhodesiense, qui est retrouvé en Afrique de l’Est, sont indistinguables morphologiquement. Des techniques de biologie moléculaire permettent de les différencier.
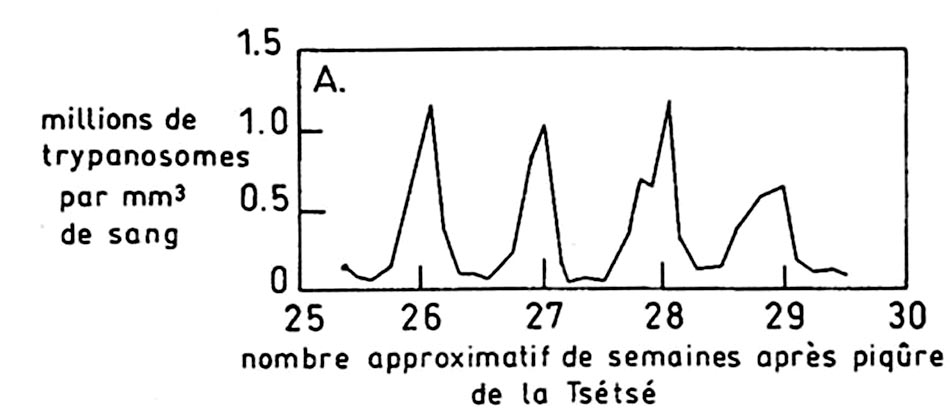
Fait capital, les trypanosomes sont recouverts d’une glycoprotéine de surface variable. Le remplacement d’une glycoprotéine de surface par une autre antigéniquement différente, entraîne le phénomène de variation antigénique. Chez l’homme infecté, des vagues de parasitémies se succèdent, chacune correspondant à un variant antigénique.
L’organisme élabore des réponses immunitaires spécifiques malheureusement inefficaces contre un parasite qui lui échappe. Cette variation antigénique handicape considérablement la réalisation d’un vaccin. De plus, cette glycoprotéine de surface induit la production excessive et prolongée de cytokines (TNF- α , IL-1) favorisant une inflammation chronique et persistante, et, probablement, l’apparition d’auto-anticorps.