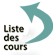- Pré-requis et Objectifs
- Cours
- Evaluations
- Annexes
3 - Filariose à Loa loa ( Loase ou Loaose)
La filariose à Loa loa, strictement africaine, est une helminthose cutanée par la localisation des vers adultes, et sanguicole par celle des embryons, ou microfilaires. Spectaculaire par quelques signes cliniques, elle peut évoluer vers des complications viscérales.
Figure 20 : Filaire adulte de Loa loa (2 à 7 cm)
3 . 1 - Épidémiologie
La filaire Loa loa est un parasite de l’homme. Les adultes sont des vers ronds, blanchâtres, de 2 à 7 cm de long : ils vivent sous la peau et leur longévité peut dépasser 15 ans. La femelle émet des embryons ou microfilaires, qui circulent dans le sang périphérique surtout le jour (microfilarémie de périodicité diurne).
Le vecteur est un taon, le chrysops (C. dimidiata et/ou C. silacea), ou « mouche rouge » ou « mouche filaire », qui abonde dans la canopée des forêts chaudes et humides d’Afrique équatoriale ; les femelles hématophages, attirées par les fumées des feux de bois, piquent le jour avec un maximum d’agressivité vers midi. En prenant leur repas sanguin chez un malade, les chrysops absorbent des microfilaires sanguicoles qui se transforment en larves infestantes en 10 à 12 jours. Au cours d’une nouvelle piqûre, les larves infestantes s’échappent de la trompe de l’insecte et traversent activement la peau d’un nouveau sujet. Au bout de trois mois, elles deviennent adultes, capables d’émettre des microfilaires.
Figure 21 : Chrysops sp. Tabanidé vecteur de la Loaose
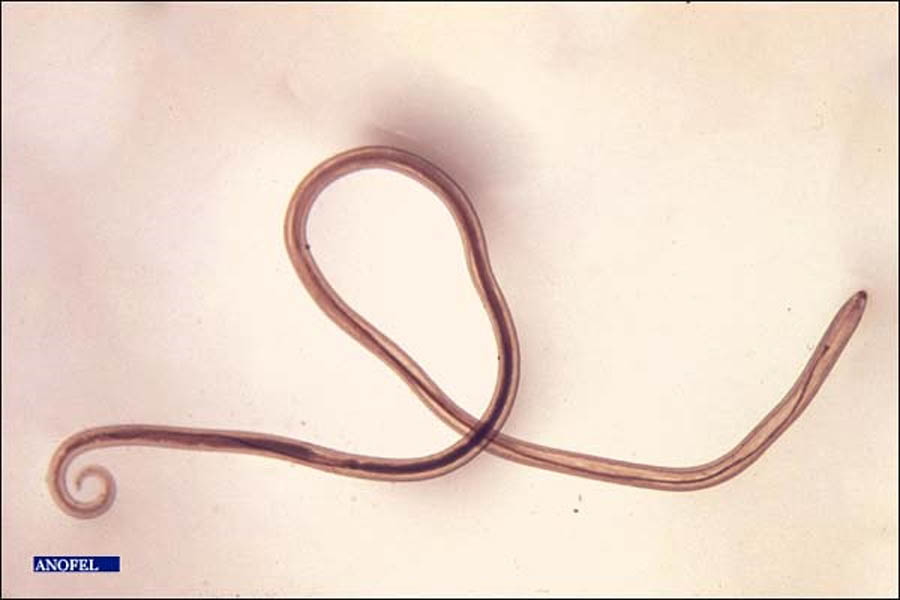
RÉPARTITION GÉOGRAPHIQUE
La loase est strictement africaine, surtout équatoriale et occidentale, limitée à la grande forêt, elle sévit de la Guinée au nord jusqu’en Ouganda à l’Est, sans atteindre l’Océan Indien. Les zones d’hyper-endémie sont le Cameroun, le Nigéria, le Gabon, le Congo Brazzaville et le Congo Kinshasa. Dans ces pays, les taux d’infestation peuvent atteindre 35 % de la population. Sa prévalence est estimée à une dizaine de millions d’individus
3 . 2 - Symptomatologie
Spectaculaire par quelques signes cliniques correspondant à la migration du ver adulte et aux réactions allergiques, la loaose peut progressivement se compliquer par des réactions immunologiques associées à l’hyperéosinophilie, touchant les endothéliums cardiaques, rénaux et cérébraux. Ces complications graves sont accentuées par des thérapeutiques mal conduites.
Après une phase d’incubation muette supérieure à trois mois, dans une population souvent asymptomatique, trois symptômes peuvent survenir, isolés ou groupés :
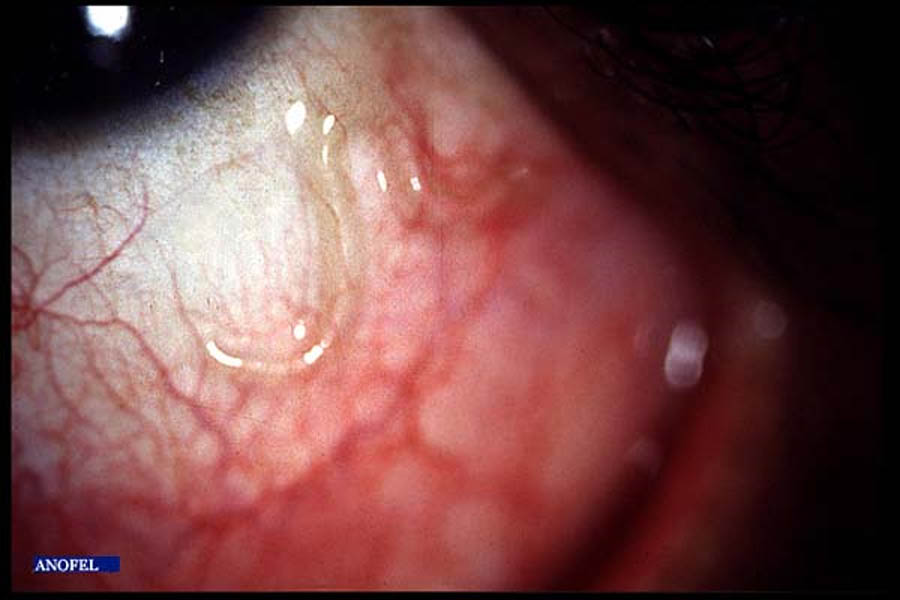
1) Passage du ver adulte sous la conjonctive
L’incident est bénin et relativement fréquent. Le ver peut passer sous la conjonctive palpébrale ou bulbaire ou sous la peau des paupières ; il peut également changer d’œil, en cheminant sous la peau à la racine du nez. La traversée rétro-conjonctivale est brève, quelques minutes, rarement davantage ; il est alors facile d’extraire la filaire. Le passage s’accompagne de photophobie, injection conjonctivale, larmoiement, sensation de corps étranger et œdème péri-orbitaire.
Chez les forts porteurs de microfilaires ont a pu décrire des atteintes hémorragiques de la paupière et des hémorragies rétiniennes.
Des cas exceptionnels de passage de filaire adulte dans la chambre antérieure de l’œil ont été décrits.
2) Reptation du ver adulte sous la peau
Elle se traduit par un fourmillement désagréable ou un prurit localisé. Le ver apparaît sous forme d’un cordon palpable, mobile, se déplaçant d’un centimètre environ par minute. Lors d’un traitement par la diéthylcarbamazine, cet incident est fréquent, les vers adultes remontant à la surface de la peau sous l’effet du médicament.
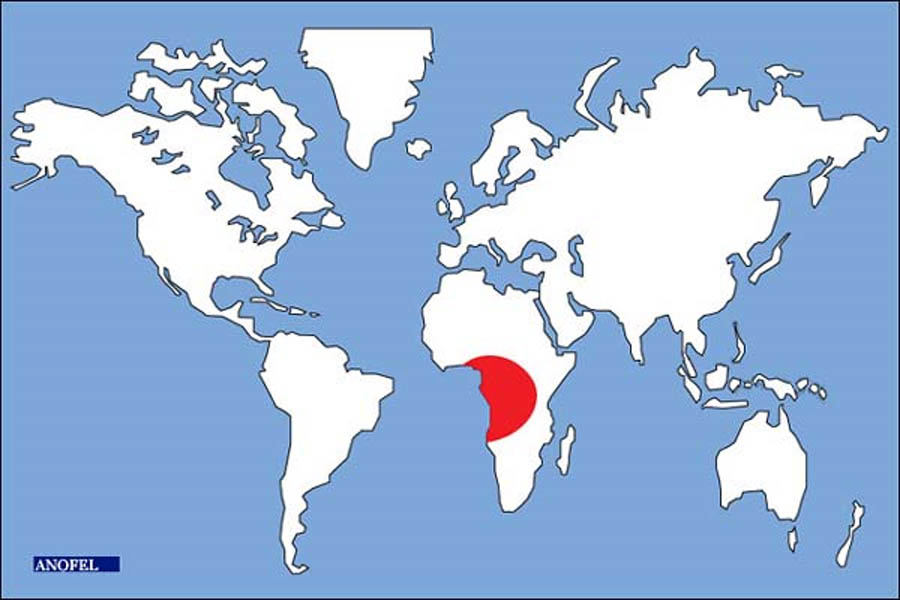
3) Œdème de Calabar
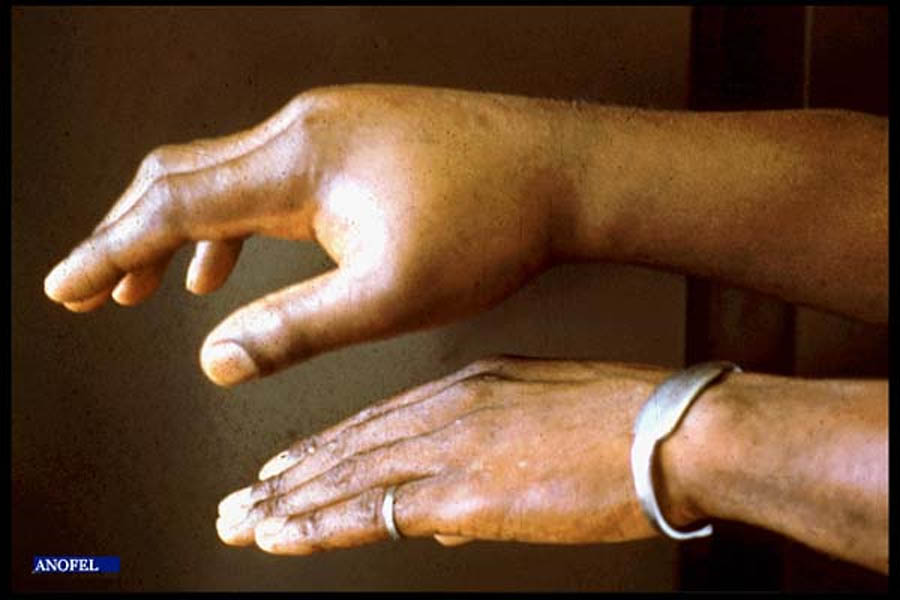
Œdème allergique, l’œdème de Calabar (localité du Nigéria en zone biafraise) est fugace et migrateur ; il dure de quelques heures à quelques jours, s’accompagne d’une sensation de tension et siège surtout aux membres supérieurs (bras, coude, poignet, main), à la face ou au thorax.
Des épisodes rares de lymphadénites, d’hydrocèles, de polyarthrites, de manifestations pulmonaires ont été rattachés à la Loaose.
Figure 23 : Œdème de Calabar, allergique fugace et migrateur pathognomonique de la filariose à Loa loa
Figure 24 : Migration sous conjonctivale d’une filaire adulte de Loa loa
En plus des manifestations classiques, trois complications sont attribuées à la loaose : la pathogénicité est discutable devant la survenue tardive de ces complications, à un moment où les parasites sont souvent absents. Ces complications restent souvent liées aux traitements mal conduits et sont :
- Complications neurologiques
Des observations d’hémiplégie, de méningite, d’encéphalite, ont été rapportées. L’encéphalite déclenchée ou majorée par un traitement intempestif par la diéthylcarbamazine ou plus rarement par l’ivermectine, lorsque la microfilarémie est intense, est un fait confirmé. La lyse brutale des microfilaires entraîne des accidents allergiques et des complications neurologiques parfois dramatiques qui, même lorsqu’elles sont transitoires, peuvent laisser des séquelles (dysarthrie).
L’altération de la barrière méningée par une affection non parasitaire (méningite tuberculeuse) peut entraîner le passage de microfilaires Loa loa dans le LCR sans pouvoir parler pour autant de syndrome méningé filarien (sans doute exceptionnel).
Dans les zones d’infections mixtes onchocercose-loase, les programmes de lutte contre l’onchocercose fondés sur la distribution d’ivermectine à toute la population doivent prendre en compte le risque de complications chez les très fort porteurs de microfilaires Loa loa sanguicoles.
- Complications cardiaques
L’endocardite pariétale fibroplastique éosinophilique de Löeffler est une affection moins rare en Afrique qu’en Europe. Elle réalise le tableau d’une insuffisance cardiaque globale, surtout droite, d’apparence primitive, avec éosinophilie sanguine élevée.
D’origine carentielle, bactérienne, virale ou parasitaire, la fibrose endocardique serait une manifestation allergique répondant souvent à l’allergène helminthique. La loase est la parasitose la plus souvent en cause mais il n’est pas toujours aisé d’en apporter la preuve car la fibrose endocardique est une complication qui survient tardivement. Les microfilaires peuvent être absentes du sang périphérique et les méthodes immunologiques sont alors une orientation précieuse.
- Complications rénales
Des néphropathies ont été décrites dans la loase. Il est souvent difficile d’affirmer que celle-ci est seule en cause dans leur genèse ; une protéinurie après plusieurs années d’infestation parasitaire, le grand nombre de microfilaires observées dans les glomérules et les capillaires du tissu interstitiel, l’élévation transitoire de la protéinurie au début du traitement spécifique, l’amélioration parfois constatée après traitement, plaident en faveur de cette relation. Les lésions anatomiques sont celles des néphrites interstitielles et les altérations des parois capillaires glomérulaires sont du même type que celles rencontrées dans d’autres néphropathies
La pathogénie est discutée : traumatique, due au passage des microfilaires en dehors des capillaires ; mécanique, due à l’obstruction des capillaires glomérulaires par les microfilaires ; ou surtout immunitaire, provoquée par l’antigénicité des matériaux libérés par la lyse des microfilaires. La preuve en serait apportée par la mise en évidence dans les dépôts extra-membraneux, grâce aux techniques d’immunofluorescence, d’antigène Loa loa, d’immunoglobulines et de complément.
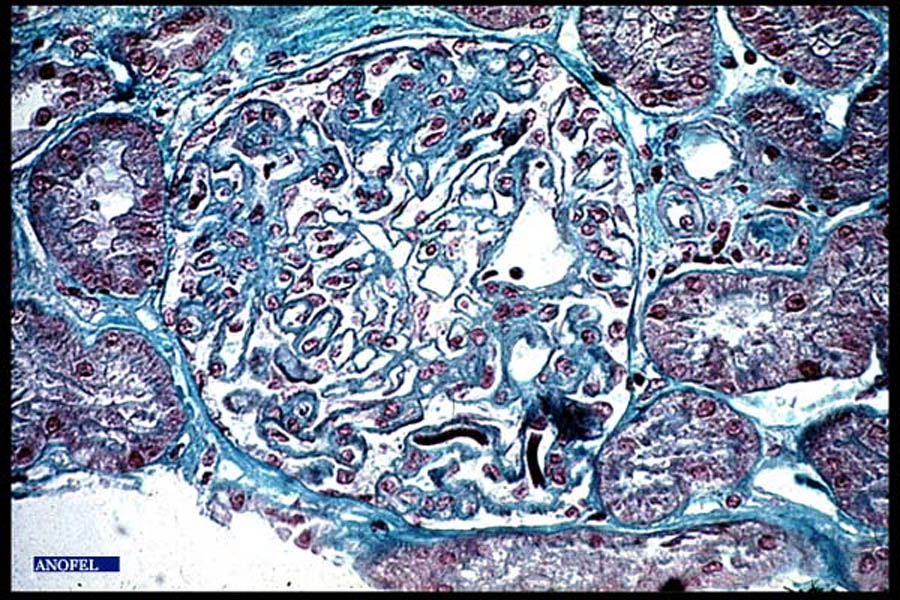
Figure 25 : Complications : Présence de microfilaires de Loa loa dans l’espace glomérulaire (coupes longitudinales et sections) coloration trichrome de Masson
7/9