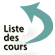2
-
Faire le diagnostic de mutation dans le gène MFR1
2
.
1
-
Tableau clinique du syndrome de l’X fragile
2
.
1
.
1
-
Généralités
Seuls les sujets ayant une mutation complète ont un tableau clinique de syndrome de l’X fragile, à des degrés divers. Ces signes cliniques sont toutefois inconstants et non pathognomoniques.
Le syndrome de l’X fragile est sous-diagnostiqué. Il peut être porté tardivement en raison de la méconnaissance du syndrome résultant, et de la variabilité des formes cliniques.
2
.
1
.
2
-
X fragile chez les garçons porteurs d’une mutation complète
Avant la puberté :
- retard de développement psychomoteur ;
- déficit intellectuel avec troubles des apprentissages (notamment langage) ;
- troubles du comportement (colère, hyperactivité, troubles autistiques) ;
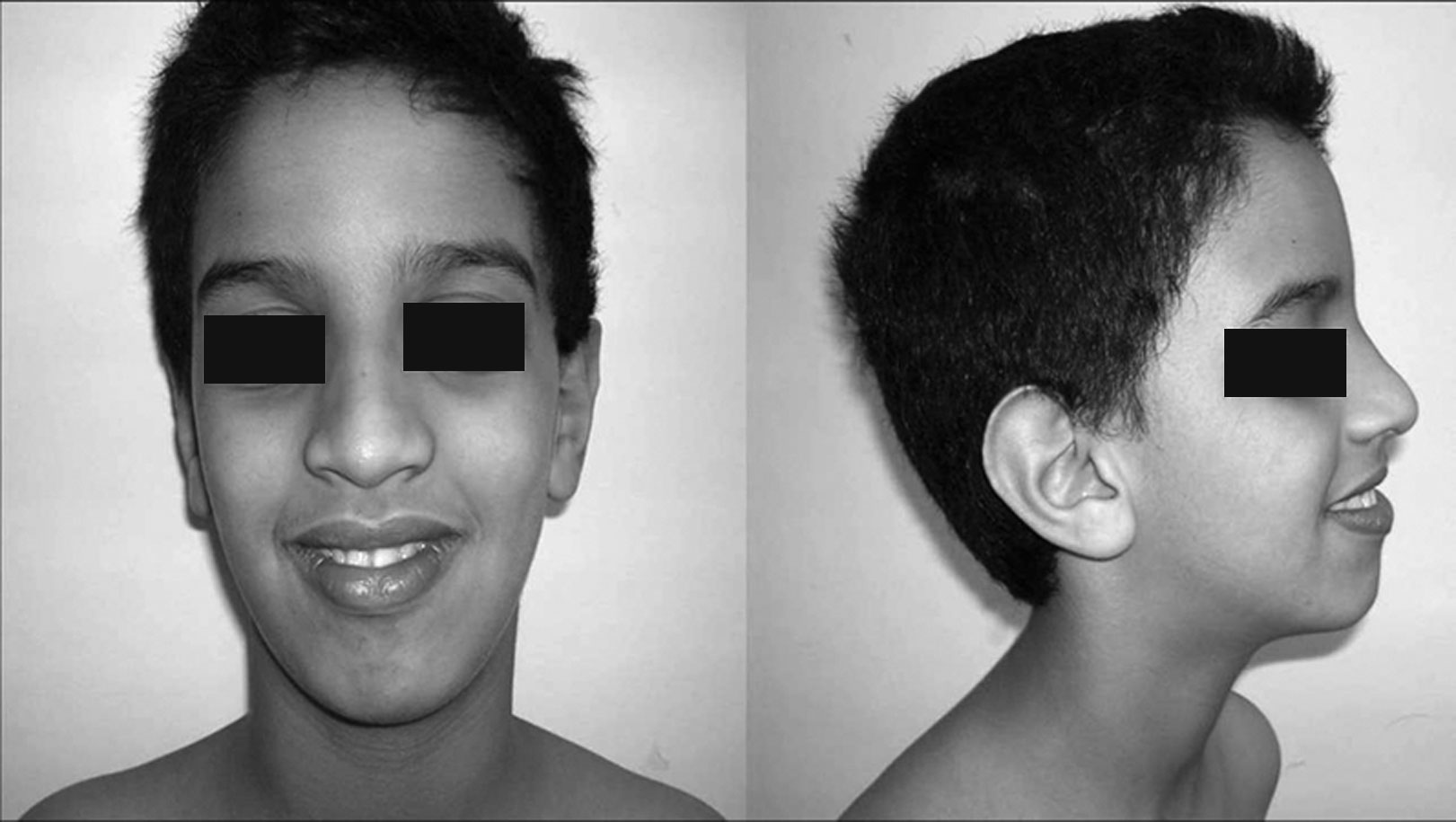
- dysmorphie faciale (fig. 12.1) :
-- visage allongé avec de grandes oreilles décollées,
-- macrocéphalie, front allongé, menton long et marqué.
Après la puberté :
- macro-orchidie ;
- dysmorphie faciale plus marquée ;
- troubles de la relation (timidité, éviction du regard) ;
- strabisme, hyperlaxité ligamentaire, prolapsus de la valve mitrale…
Triade inconstante = déficit intellectuel, dysmorphie faciale, macro-orchidie (après la puberté).
2
.
1
.
3
-
X fragile chez les filles porteuses d’une mutation complète
La plupart des signes observés chez les garçons ont aussi été décrits chez les filles. Ils sont en revanche moins fréquents et plus modérés.
Une déficience mentale est rapportée chez les filles dans 50 % des cas, avec une expression plus modérée que chez les garçons. Dans 50 % des cas, l’intelligence est tout à fait normale. Cette variation interindividuelle chez les filles s’explique par le phénomène d’inactivation de l’X.
Déficit intellectuel si mutation complète = 100 % des garçons et 50 % des filles.
2
.
2
-
Conséquences cliniques d’une prémutation dans le gène FMR1
2
.
2
.
1
-
Généralités
La prémutation ne donne pas de syndrome de l’X fragile.
Les personnes porteuses d’une prémutation sont en revanche à risque de développer : des troubles neurologiques tardifs (Fragile X Tremor Ataxia Syndrome [FXTAS]) pour les hommes (mais également les femmes), et un syndrome d’insuffisance ovarienne (Premature Ovarian Failure [POF]) pour les femmes. Ces troubles n’apparaissent qu’à l’âge adulte.
2
.
2
.
2
-
Prémutation chez les hommes
La prévalence du syndrome FXTAS est de l’ordre de 40 % après l’âge de 50 ans.
Il est caractérisé par un tremblement d’intention et une ataxie cérébelleuse de début tardif et progressif.
D’autres atteintes neurologiques peuvent s’associer : troubles de la mémoire à court terme, altération des fonctions exécutives et cognitives, démence, syndrome de Parkinson, neuropathie périphérique, déficit moteur proximal des membres inférieurs et dysfonction du système autonome.
2
.
2
.
3
-
Prémutation chez les femmes
La prévalence du POF est de l’ordre de 21 % (versus 1 % dans la population générale).
Il se caractérise par une ménopause précoce (arrêt des menstruations avant l’âge de 40 ans). Cela peut être parfois le signe révélateur de l’anomalie du gène FRM1 au sein d’une famille.
La prévalence du risque de FXTAS chez ces femmes n’est pas encore déterminée.
Prémutation : prédisposition à FXTAS et POF, pas de tableau d’X fragile.
2
.
3
-
Examens paracliniques
2
.
3
.
1
-
Généralités
La suspicion clinique doit être confirmée par des examens génétiques.
La biologie moléculaire est actuellement la méthode diagnostique de référence.
L’étude cytogénétique a permis l’individualisation de ce syndrome ; mais ses résultats sont peu fiables.
2
.
3
.
2
-
Génétique moléculaire
La PCR permet d’amplifier l’ADN et d’évaluer le nombre de triplets CGG au sein du gène FMR1.
Le Southern Blot étudie l’ADN sans amplification et permet de déterminer le statut de méthylation ainsi que de caractériser les grandes expansions de triplets ne pouvant pas être étudiées par PCR pour des questions de limite technique.
2
.
3
.
3
-
Étude cytogénétique
Initialement, le diagnostic était fait par étude cytogénétique (caryotype). Le caryotype reste toutefois indiqué car il peut mettre en évidence une autre cause de déficit intellectuel.
La mise en évidence d’une cassure de l’extrémité distale des bras longs du chromosome X au niveau du site fragile FRAXA permet un diagnostic positif. Toutefois, il existe des faux négatifs et des faux positifs.
Biologie moléculaire (PCR puis Southern Blot) = confirmation diagnostique.
Caryotype = intérêt pour mettre en évidence une autre cause de déficit intellectuel.
2/5