2
.
4
-
Conduire l’enquête étiologique
2
.
4
.
1
-
Enquête clinique minutieuse
Anamnèse
- Éléments du dossier obstétrical (si nouveau-né) et antécédents familiaux :
- hémoglobinopathie, enzymopathie, anomalies de membrane du globule rouge ;
- carence martiale maternelle, multiparité, prématurité, RCIU.
- Terrain :
- âge, sexe, origine ethnique, croissance staturo-pondérale (cassure) ;
- antécédents personnels de maladie chronique, œsophagite, ulcère.
- Mode de vie :
- prise de médicaments (aspirine, AINS…) ou de fèves, voyage à l’étranger ;
- allaitement maternel prolongé, régime pauvre en fer, pica, ingestion de peinture au plomb.
- Mode d’installation de l’anémie :
- mode de révélation, date de début des symptômes ;
- rapidité de constitution de l’anémie et retentissement cardiorespiratoire.
- Signes fonctionnels :
- diarrhée chronique, anorexie, dégoût de la viande, épigastralgies ;
- épistaxis répétées, règles abondantes, saignement aigu.
Examen physique
- Signes de sévérité symptomatique et de cause potentiellement grave :
- cause tumorale : adénopathies, hépatosplénomégalie, purpura, fièvre ;
- hémolyse aiguë : urines rouges (hémoglobinurie), signes généraux liés à l’hémolyse elle-même (frissons, fièvre, douleurs lombaires).
- Autres signes à rechercher :
- signes de carence martiale : ongles mous, perlèche, glossite, infections ;
- signes de pathologie auto-immune ou inflammatoire.
- Deux tableaux cliniques distincts permettent d’orienter l’enquête étiologique d’une anémie hémolytique :
- hémolyse aiguë : urines rouges en rapport avec l’hémoglobinurie, subictère et splénomégalie peu marquée ; risque de complication aiguë (insuffisance rénale avec oligo-anurie par précipitation tubulaire d’hémoglobine, malaise, voire choc anémique) ;
- hémolyse chronique : urines foncées, ictère marqué, splénomégalie volumineuse avec risque de complication par lithiase biliaire.
Rechercher : urines foncées, ictère, syndrome tumoral, purpura.
2
.
4
.
2
-
Enquête paraclinique orientée
Paramètres à considérer en priorité devant une anémie
- Réticulocytes :
- réticulocytes < 50–100 g/L : anémie arégénérative ou peu régénérative ;
- réticulocytes > 120 g/L : anémie régénérative.
- Volume globulaire moyen (VGM) :
- VGM < 80 fL : anémie microcytaire ;
- VGM > 100 fL : anémie macrocytaire.
À noter que le nouveau-né a une macrocytose physiologique, puis le VGM diminue rapidement (on définit la microcytose pour un VGM < 70 fl chez le nourrisson). Le VGM augmente ensuite pour rejoindre très progressivement les normes adultes vers l’âge de 10 ans.
Autres examens effectués selon l’orientation clinique
- En cas d’anémie microcytaire :
- bilan martial : ferritine (en 1re intention), fer, transferrine ;
- bilan inflammatoire : VS, CRP ;
- électrophorèse de l’hémoglobine, dosage du plomb (en 2e intention).
- En cas d’hémolyse aiguë :
- frottis sanguin : anomalies morphologiques du globule rouge → recherche de schizocytes, recherche de parasites (paludisme) en cas de voyage en pays d’endémie ;
- test de Coombs : AHAI (anémie hémolytique auto-immune) ;
- dosage de la G6PD ;
- créatinémie, protéinurie.
- En cas d’hémolyse chronique :
- test de Coombs : AHAI ;
- étude des différents compartiments du globule rouge en rapport avec une cause corpusculaire d’hémolyse : membrane, enzymes (pyruvate kinase), électrophorèse de l’hémoglobine.
À noter que plusieurs causes d’anémie peuvent être intriquées ; ce qui peut rendre parfois l’interprétation des paramètres biologiques difficiles (ex. : hémolyse constitutionnelle et carence martiale).
Orientation diagnostique : contexte clinique, VGM et réticulocytes.
2
.
4
.
3
-
Principales causes d’anémie chez l’enfant
Une anémie est schématiquement due :
- à des causes centrales (arégénératives) :
- insuffisance médullaire d’origine carentielle (défaut de production),
- envahissement ou aplasie médullaire ;
- à des causes périphériques (régénératives) :
- hémolyse (excès de destruction),
- hémorragie (perte excessive).
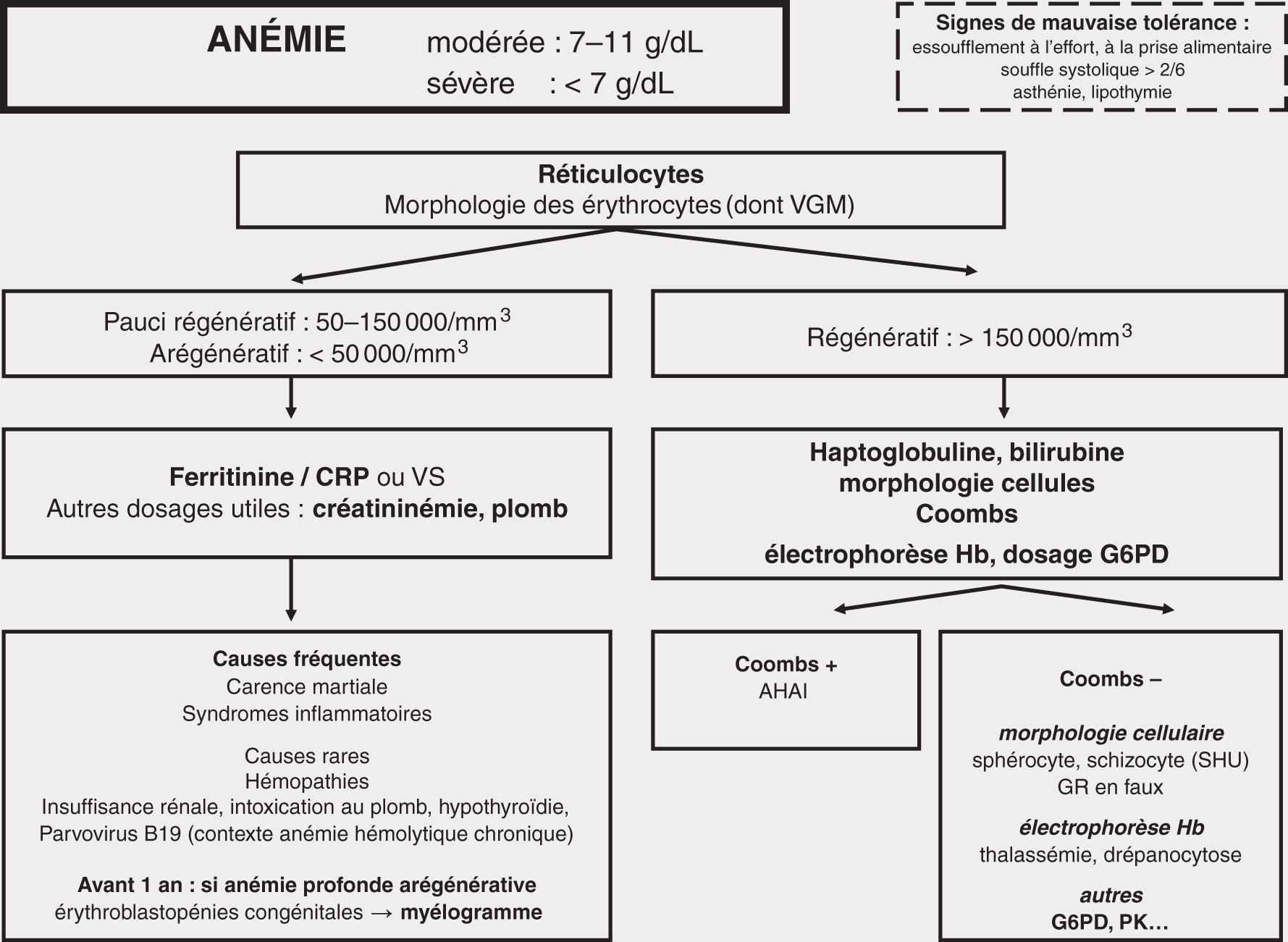
L’arbre diagnostique proposé figure 42.1 permet de schématiser la conduite diagnostique et de synthétiser les causes d’anémie en pédiatrie.
L’ensemble des causes d’anémie ne sont pas détaillées dans ce chapitre.
Certaines anémies hémolytiques du nouveau-né sont explicitées dans le chapitre 2.
Les points clés de la carence martiale et de la drépanocytose seront traitées ci-dessous.
La thalassémie bêta homozygote ou maladie de Cooley représente un tableau tout à fait spécifique du très jeune enfant. Le diagnostic est porté entre les âges de 6 et 24 mois, dans un contexte d’anémie sévère arégénérative et d’hémolyse par dysérythropïèse. Le tableau clinique est marqué par un ictère intense, une splénomégalie très volumineuse et des déformations osseuses.
2
.
5
-
Savoir prescrire une transfusion de CGR
La décision de transfuser un enfant doit prendre en compte :
- la tolérance clinique ;
- la profondeur de l’anémie ;
- le risque d’aggravation (hémorragie ou hémolyse actives) et le potentiel de récupération rapide (réticulocytose).
Les grands principes de transfusion de CGR sont proches de ceux appliqués chez l’adulte. Nous ne rappelons ici que les messages essentiels pour la pratique clinique.
- Avant la transfusion :
- connaître les antécédents de transfusion de l’enfant (nombre, accidents éventuels) ;
- information des parents ± de l’enfant sur le rapport bénéfices/risques, accord parental ;
- bilan prétransfusionnel (± éventuels prélèvements à visée étiologique).
- Commande des culots globulaires :
- nom, prénom, âge, poids de l’enfant, chiffre d’hémoglobine, tolérance clinique ;
- date, identification du prescripteur, signature, degré d’urgence ;
- quantité à transfuser = ΔHb × 3–4 × poids en kg (sans dépasser 20 mL/kg) ;
- systématiquement : isogroupe et iso-Rhésus, déleucocytés ;
- particularités : phénotypés si transfusions itératives, compatibilisés si RAI +, irradiés si hémopathie en cours de traitement, greffé ou autre déficit immunitaire.
- Modalités de la transfusion :
- contrôle ultime au lit : concordance de l’identité, méthode de Beth-Vincent ;
- durée de transfusion : 4 heures en règle générale ;
- surveillance rapprochée des paramètres vitaux (température, hémodynamique, conscience).
- Après la transfusion :
- traçabilité : notification dans les dossiers transfusionnel et médical ainsi que le carnet de santé ;
- vérification de l’efficacité de la transfusion : examen clinique, NFS de contrôle (retenir que : 3–4 mL/kg de CGR élèvent habituellement l’hémoglobine de 1 g/dL) ;
- bilan post-transfusionnel : RAI à 3 mois (sérologies virales non recommandées).
Transfusion : CGR isogroupes déleucocytés, Beth-Vincent, surveillance clinique, NFS.
3/7