1 - Introduction
Tous les matériaux qui nous entourent sont formés d’atomes et de molécules. L’arrangement et la relation qui existent entre ceux-ci expliquent certaines de leurs propriétés. Pendant longtemps les physiciens, en se fondant sur l’apparence immédiate des corpsDéfinitionwww.techno-science.net.Un corps pur est composé d'un seul type de constituant (contraire : mélange).Corps pur élémentaire : corps constitué d'atomes d'une seule sorte, mais non associés en molécules. Ex : Cuivre (Cu).Corps pur simple : Corps constitué d'atomes d'une seule sorte, associés en molécules . Ex : Hydrogène (H2).Corps pur composé : Corps constitué de molécules constituées à partir d'atomes de plusieurs sortes. Ex : eau H2O.Corps pur atomique : corps dont on ne voit pas les différent contituantsIl ne faut pas confondre un mélange (par exemple le gaz constitué d'hydrogène et d'oxygène) avec de l'eau (qui est le résultat de la réaction chimique de combustion).Dans le mélange, chaque gaz a un comportement propre. Dans l'eau, toute la vapeur (ou le liquide) se comporte de façon identique. Il ne faut pas confondre non plus la notion d'élément chimique et de corps pur. qui nous entourent, ont distingué les états solide, liquide et gazeux. La classification actuelle repose sur la structure atomique des matériaux et ne considère plus que deux états principaux : l’état désordonné et l’état ordonné (Figure 1).
Rem : Le solide est dur et ne se déforme pas. Au contraire, un liquide et un gaz se déforment, ils prennent la forme du récipient dans lequel on les place ; Le solide, placé régulièrement, forme des cristaux. Dans un cristal, il y a donc un ordre.
Dans l’état désordonné, les atomes ou molécules constituant la matière sont disposés de façon essentiellement aléatoire. Les gaz et les liquides de l’ancienne classification appartiennent naturellement à cette catégorie, mais aussi les solides amorphes, tels que les verresDéfinitionwww.techno-science.net.Dans le langage courant, le mot verre sert à désigner un matériau dur, fragile (cassant) et transparent.Dans le langage scientifique, le mot verre est un matériau amorphe (c'est-à-dire non cristallin) présentant le phénomène de transition vitreuse. L’état physique résultant est appelé état vitreux. Le plus souvent, le verre est constitué d’oxyde de silicium (silice SiO2) et de fondants. ou certains polymèresDéfinitionhttp://fr.wikipedia.org/.Le mot polymère vient du grec polus plusieurs, et meros parties.Un polymère est une substance organique ou inorganique, liquide ou solide à température ambiante, constituée d'enchaînements en motifs répétés de macromolécules de même nature chimique et reliées par des liaisons covalentes. Un polymère peut être d'origine naturelle, ou obtenu par modification chimique d'un polymère naturel, ou bien entièrement synthétisé par voie chimique ou enzymatique par une réaction de polymérisation. Ces réactions de polymérisation, établissant des liaisons covalentes entre de petites molécules monomères (du grec monos: un seul ou une seule, et meros ; partie), conduisent à la formation de macromolécules ayant une structure tridimensionnelle. Les macromolécules dont les polymères sont constitués peuvent présenter des masses moléculaires (on devrait dire en fait masses molaires) variées ; la masse moléculaire d'un polymère est donc la moyenne de celle des macromolécules qui le constituent. , qui peuvent être en fait considérés comme des liquides de viscositéDéfinitionhttp://fr.wikipedia.org/wiki/Viscosit%C3%A9.La viscosité (du latin viscum) désigne la capacité d'un fluide à s'écouler, en mécanique des fluides. En langage courant, on utilise aussi le terme de fluidité.Lorsque la viscosité augmente, la capacité du fluide à s'écouler diminue. La viscosité tend à diminuer lorsque la température augmente. Par contre, on pourrait croire que la viscosité d'un fluide s'accroît avec sa densité mais ce n'est pas nécessairement le cas. très élevée. A l’opposé, dans l’état ordonné ou cristallinDéfinitionhttp://fr.wikipedia.org/wiki/Syst%C3%A8me_cristallin.Un système cristallin est un classement des cristaux sur la base de leurs caractéristiques de symétrie, sachant que la priorité donnée à certains critères plutôt qu'à d'autres aboutit à différents systèmes.La symétrie de la maille conventionnelle permet de classer les cristaux en différentes familles cristallines : quatre dans l'espace bidimensionnel, six dans l'espace tridimensionnel.Une classification plus fine regroupe les cristaux en différents systèmes. Il existe deux types de systèmes, selon que le critère de classification est la symétrie du réseau ou la symétrie morphologique. Historiquement, ces deux systèmes ont été indistinctement appelés système cristallin, ce qui a été à l'origine de la confusion dans la littérature surtout minéralogique. , les éléments constitutifs (atomes, ions ou molécules) sont répartis de façon régulière suivant les trois directions de l’espace. Ces matériaux sont parfois qualifiés de « vrais solides ». La plupart des objets qui nous entourent relèvent de cette catégorie.
Dans certains cas, peu fréquents, les solides cristallins apparaissent sous la forme de monocristaux : quartz, pierres précieuses, etc. L’ordre tridimensionnel se manifeste alors par leur aspect géométrique : faces planes se coupant suivant des arêtes vives et faisant entre elles des angles bien déterminés.
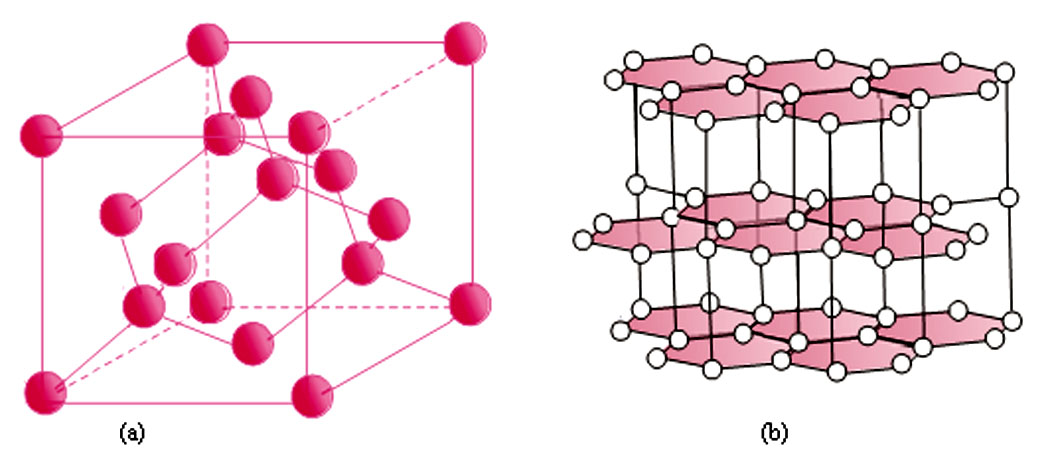
Ex : le diamant est formé de carbone comme le charbon mais dans le charbon, le carbone est placé irrégulièrement. La différence entre le diamant et le graphite, également formé de carbone est la disposition des atomes et des plans cristallins (Figure 2 ).
Le plus souvent, en revanche, les matériaux cristallins sont des agrégats d’une multitude de cristaux parfois très petits (de quelques microns à quelques centaines de microns). Dans ces polycristaux, le caractère ordonné de la matière, présent à l’échelle de chaque cristal, n’apparaît plus au niveau macroscopique. Les métauxDéfinitionhttp://fr.wikipedia.org/wiki/M%C3%A9tal.Un métal est un élément chimique qui peut former des liaisons métalliques et perdre des électrons pour former des cations (ions positifs) (et des liaisons ioniques dans le cas des alcalins). Les métaux sont un des trois groupes d'éléments distingués par leurs propriétés d'ionisation et de liaison chimique ; les deux autres sont les métalloïdes et les non-métaux.Dans le tableau périodique des éléments la diagonale partant du bore (B) et allant jusqu'au polonium (Po) sépare les éléments métalliques (en bas à gauche) des éléments non métalliques (en haut à droite). Les éléments placés sur cette ligne sont des métalloïdes.De plus, le caractère métallique des éléments d'une même colonne augmente avec le nombre d'électrons (c'est-à-dire lorsque l'on descend dans le tableau). Par exemple, le carbone-diamant (Z=6) est un isolant, le silicium (Z=14) est un semi-conducteur et l'étain (Z=50) est un métal. et les alliagesDéfinitionhttp://fr.wikipedia.org/wiki/Alliage.Un alliage est une combinaison d'un métal avec un ou plusieurs autres éléments.Un métal pur a des caractéristiques mécaniques relativement faibles. Le fait d'ajouter d'autres éléments permet de durcir (augmenter les caractéristiques mécaniques) et/ou de modifier les caractéristiques chimiques des métaux (en particulier leur comportement à la corrosion), ou d'améliorer d'autres caractéristiques (facilité de mise en œuvre : coulabilité par exemple).Le métal principal est appelé le métal de base ou la base. Les éléments ajoutés volontairement sont appelés les éléments d'alliage (ou d'addition) et les éléments non désirés sont appelés les impuretés.Les éléments d'alliages sont le plus souvent des métaux mais ils peuvent également être d'autres éléments chimiques (exemples : le carbone dans l'acier ou la fonte, le silicium dans l'aluminium, ...).Généralement, quand l'élément d'alliage n'est pas un métal, sa proportion reste faible. La concentration de carbone est inférieure à 2% en masse pour l'acier et inférieure à 6% en masse pour la fonte, alors qu'il est possible de faire un alliage Cuivre Zinc (laiton) avec 50% de chacun des éléments.Un alliage peut être naturel, c'est rare mais ça existe, par exemple l'électrum alliage d'or et d'argent natifs utilisé dans la préhistoire et l'antiquité : Varna, Anatolie, Ur, Égypte etc. métalliques relèvent de cette description, de même que les céramiquesDéfinitionhttp://fr.wikipedia.org/wiki/C%C3%A9ramique.Premier art du feu à apparaître (avant la métallurgie puis le travail du verre), la céramique désigne l’ensemble des objets fabriqués en terre qui ont subi au cours d’une cuisson plus ou moins élevée, une transformation physico-chimique irréversible.Le mot céramique provient du grec ancien kéramos, qui signifie terre à potier, argile. Il a donné son nom à un quartier d'Athènes, le Céramique.On peut distinguer trois branches de la céramique :• la céramique utilitaire, principalement la poterie, la plus ancienne des formes de céramique (elle est antérieure au travail des métaux) qui utilise les terres argileuses comme matériau de base ;• la céramique d'art qui a dérivé de la précédente, et délaisse la fonction utilitaire pour se centrer sur le sens mystique ou sur l'esthétique ;• la céramique industrielle, particulièrement développée au XXe siècle et qui utilise des matériaux à base d'oxydes, de carbures, de nitrures, etc.Un matériau céramique est solide à température ambiante et n'est ni métallique, ni organique. Les objets en céramique sont réalisés par solidification à haute température d'une pâte humide plastique, ou agglutination par chauffage (frittage) d'une poudre sèche préalablement comprimée, sans passer par une phase liquide ; par extension, on désigne sous le terme « céramique » les objets eux-mêmes ainsi fabriqués. et certains polymères partiellement cristallins. Dans le cas des métaux, les cristaux de l’agrégat sont appelés grains et les frontières entre ces cristaux joints de grains (cf. Arrangement structural des solides cristallins).
La disposition des atomes ou des groupes d’atomes dans un solide cristallin, c’est-à-dire la structure cristalline de l’ensemble, dépend de plusieurs facteurs, en particulier du type de liaison entre les atomes (cf. Les liaisons atomiques) et du nombre de premiers voisins, ou nombre de coordinence, que chaque atome peut accepter.
→ Le nombre de premiers voisins est le nombre d’atomes en contact avec un atome pris comme origine.




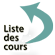

.jpg)