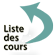1 . 3 . 2 - Diagnostic étiologique
a. Causes d’insuffisance surrénale basse (maladie d’Addison)
Origine auto-immune : rétraction corticale
L’origine auto-immune concerne environ 80 % des cas, c’est donc de loin la cause la plus fréquente.
Elle est plus fréquente chez la femme que chez l’homme (sex-ratio de 3/1).
On retrouve fréquemment des antécédents familiaux de maladies auto-immunes.
La maladie d’Addison peut être isolée ou associée à d’autres maladies auto-immunes :
- thyroïdite de Hashimoto (syndrome de Schmidt) +++ ;
- diabète de type 1 ;
- insuffisance ovarienne prématurée (ménopause précoce) ;
- vitiligo, etc.
Deux syndromes ont été bien caractérisés (voir p. 358, tableau 17.II) :
- la polyendocrinopathie auto-immune de type 1, de transmission autosomique récessive, liée à une mutation du facteur de transcription AIRE (hypoparathyroïdie, candidose, insuffisance surrénale et, plus rarement, hépatite, hypogonadisme, vitiligo, alopécie, maladie de Biermer, hypothyroïdie, diabète, maladie cœliaque, etc.) ;
- la polyendocrinopathie auto-immune de type 2, de transmission autosomique dominante, dont le gène n’a pas encore été isolé (hyper ou hypothyroïdie, diabète et, plus rarement, insuffisance surrénale, myasthénie, vitiligo, maladie de Biermer, alopécie, etc.).
Des examens complémentaires peuvent être proposés :
- des auto-anticorps anti-21-hydroxylase (+++) sont retrouvés dans 80 à 90 % des cas au début de l’évolution de la maladie ; ils peuvent disparaître ensuite ;
- les surrénales apparaissent atrophiques au scanner (+++) ;
- on peut retrouver les signes cliniques et hormonaux d’une hypothyroïdie ou d’une autre pathologie auto-immune.
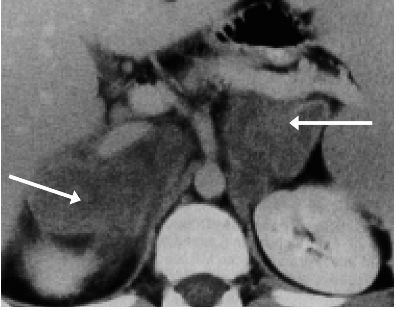
Tuberculose bilatérale des surrénales
Elle concerne environ 20 % des cas de maladie d’Addison en France.
Elle est due à une localisation du BK (bacille de Koch) dans les surrénales suite à une dissémination hématogène. Elle ne devient habituellement parlante que plusieurs années après la première localisation de la tuberculose.
Le terrain est le suivant : il s’agit souvent de sujets transplantés (provenant de pays dans lesquels la tuberculose est endémique) ou immunodéprimés, avec antécédents de tuberculose et/ou autre atteinte symptomatique de la maladie.
Des examens complémentaires peuvent être proposés :
- ASP (abdomen sans préparation) peu sensible et scanner des surrénales (+++) : les surrénales sont augmentées de taille à la phase initiale puis s’atrophient et se calcifient dans 50 % des cas (figure 18.1) ;
- la radiographie du thorax et le scanner thoracique montrent des signes de tuberculose, éventuellement au stade de séquelles ;
- un bilan des différentes localisations de la tuberculose est indispensable.
Au cours de l’infection par le VIH
Elle survient habituellement à un stade avancé de la maladie.
Les mécanismes sont multiples :
- localisation surrénalienne d’une infection opportuniste (CMV ++, toxoplasmose, BK ou mycobactérie atypique, cryptococcose ou histoplasmose) ou d’une pathologie maligne (lymphome, etc.) ;
- mécanisme iatrogène : mitotane kétoconazole, rifampicine, etc. ;
- atteinte de l’hypophyse par un lymphome ou une infection à CMV, etc.
Il faut faire attention en cas de dénutrition avec une hypoprotidémie importante car le dosage du cortisol plasmatique qui mesure le cortisol total (c’est-à-dire le cortisol lié à la CBG plus le cortisol libre, biologiquement actif) peut faire sous-estimer la fonction surrénalienne. Le diagnostic d’insuffisance surrénale dans ce contexte devra être confirmé par une évaluation du cortisol libre et nécessite un avis spécialisé.
Chez l’enfant
L’insuffisance surrénale est rare et les causes génétiques sont de loin les plus fréquentes.
Adrénoleucodystrophie
Maladie récessive liée à l’X, elle entraîne une accumulation d’acides gras à très longue chaîne, par mutation d’un gène codant pour un transporteur de ces molécules dans le peroxysome. Elle touche les garçons, dans l’enfance ou au début de l’âge adulte. La forme de l’adulte (adrénomyéloneuropathie) constitue à l’heure actuelle la troisième cause en fréquence d’insuffisance surrénale primitive. L’adrénoleucodystrophie associe une insuffisance surrénale à des troubles neurologiques d’aggravation progressive mais d’intensité et de date d’apparition variables. L’insuffisance surrénale peut au début apparaître isolée.
Bloc enzymatique (hyperplasie congénitale des surrénales)
Il s’agit de maladies autosomiques récessives liées à une mutation d’un gène codant pour une enzyme de la stéroïdogenèse. Le gène le plus souvent en cause est celui codant pour la 21-hydroxylase. Le cortisol et l’aldostérone ne sont pas synthétisés normalement, d’où l’insuffisance surrénale. Les précurseurs s’accumulent en amont du bloc et sont déviés vers la voie des androgènes, d’où une ambiguïté sexuelle chez la petite fille. Dans les formes complètes, le diagnostic est établi dans la période néonatale sur une déshydratation avec perte de sel et troubles digestifs. Le diagnostic néonatal est en train d’être généralisé en France.
Il existe des formes partielles (l’enzyme mutée a gardé une partie de son activité), révélées plus tardivement devant un hirsutisme et d’autres signes d’hyperandrogénie chez la femme, l’insuffisance surrénale étant partielle.
De façon très rare, on observe : une hypoplasie congénitale des surrénales (mutation de DAX1), une mutation inactivatrice du récepteur de l’ACTH, une hémorragie bilatérale des surrénales dans le cadre d’une méningite à méningocoque.
Autres causes surrénaliennes
Ces autres causes sont :
- iatrogènes : surrénalectomie bilatérale, anticortisolique de synthèse (Op’DDD : Lysodren®), kétoconazole (Nizoral®), etc. ;
- métastases bilatérales : cancer du poumon, cancer du rein, du sein ou ORL, etc. Le scanner montre deux masses surrénaliennes : le primitif est le plus souvent facilement retrouvé (scanner thoraco-abdominal, fibroscopie bronchique, etc.). En cas de doute, la biopsie surrénalienne peut aider (mais attention, car avant une biopsie surrénalienne il faut avoir formellement éliminé un phéochromocytome) ;
- tumeurs primitives bilatérales : lymphome (figure 18.2) ;
- maladie infiltrative : sarcoïdose, amylose, etc. ;
- causes vasculaires : nécrose des surrénales à l’occasion d’un état de choc, thrombose des veines surrénaliennes, etc.
b. Causes d’insuffisance corticotrope (voir chapitre 12)
La cause de loin la plus fréquente est l’interruption d’une corticothérapie prolongée.
Il faut habituellement une dose supraphysiologique (plus de 30 mg d’équivalent hydrocortisone, soit plus de 7 mg de prednisone, par exemple) pendant 3 à 4 semaines (en fait, grande variabilité individuelle dans la sensibilité de l’axe aux corticoïdes).
Les antécédents de corticothérapie doivent être recherchés à l’interrogatoire en sachant que d’autres voies d’administration, autres que la voie orale, peuvent être en cause : corticothérapie percutanée, intramusculaire (formes retard +++), intra-articulaire, forme inhalée.
Au cours d’une corticothérapie, l’axe hypophysosurrénalien est constamment freiné. Une décompensation peut survenir en cas de pathologie intercurrente ou en cas de dose < 5 mg d’équivalent prednisone (correspondant à 20 mg d’hydrocortisone) (tableau 18.II).
| 1/2 vie plasmatique (min) | 1/2 vie biologique (h) | Activité glucocorticoïde* |
|
| Hydrocortisone | 90 | 8-12 | 1 |
| Prednisone | 200 | 18-36 | 4 |
| Prednisolone | 200 | 18-36 | 4 |
| Bétaméthasone | 300 | 36-54 | 40 |
| Dexaméthasone | 300 | 36-54 | 40 |
Les autres causes sont :
- tumeur de la région hypothalamo-hypophysaire ;
- atteinte auto-immune (hypophysite) ;
- granulomatose (sarcoïdose en particulier) ;
- traumatisme ;
- chirurgie hypophysaire ;
- radiothérapie ;
- nécrose brutale à l’occasion d’un choc hypovolémique dans le post-partum (syndrome de Sheehan) (très rare).
Dans ces situations, le déficit corticotrope est rarement isolé. Il s’associe le plus souvent à une insuffisance d’autres axes hypothalamo-hypophysaires et/ou à des signes neurologiques (cf. chapitre 12 : « Adénome hypophysaire »).
1 . 4 - Prise en charge
Rappelons que le traitement doit avoir débuté sans attendre le résultat des dosages hormonaux. Il est du reste parfaitement possible de débuter le traitement et de faire dans un deuxième temps le test au Synacthène® ainsi que le dosage d’ACTH. Compte tenu de la durée de vie très courte de l’hydrocortisone, il suffit de faire les prélèvements avant la prise du matin.
La prise en charge comporte 4 volets :
- un traitement substitutif ;
- un traitement de la cause s’il y a lieu ;
- une éducation thérapeutique du patient ;
- une surveillance.
1. Traitement substitutif
Il associe :
- un glucocorticoïde : Hydrocortisone®, 20 à 30 mg par jour, deux tiers de la prise le matin, un tiers à midi ;
- avec un minéralocorticoïde : Fludrocortisone®, 50 à 150 mg/jour en 1 ou 2 prises.
Dans l’insuffisance corticotrope, seule l’hydrocortisone est nécessaire +++.
En cas de déficit combiné, insuffisance surrénale associée à une hypothyroïdie (par association de deux pathologies auto-immunes, ou lors d’une insuffisance antéhypophysaire).
2. Traitement de la cause
S’il y a lieu (tuberculose, métastases, autre infection, sarcoïdose, etc.) (cf. items correspondants).
3. Éducation thérapeutique du patient
L’éducation du patient concerne les points suivants :
- régime normosodé ;
- pas d’automédication (laxatifs et diurétiques en particulier) ;
- doubler la dose d’hydrocortisone en cas de fièvre ou de pathologie intercurrente ;
- augmenter la dose en cas de grossesse ;
- connaître les signes d’insuffisance surrénale ;
- avoir chez soi une ampoule d’hydrocortisone injectable de 100 mg à injecter en IM en cas de vomissements ou de malaise, ou en cas d’autre signe de décompensation surrénalienne (éduquer l’entourage +++) ;
- traitement à vie (ou jusqu’à la preuve de la récupération de l’axe hypophysosurrénalien en cas d’insuffisance corticotrope postcorticothérapie) ;
- porter sur soi une carte de traitement +++ ;
- prévenir tout nouveau médecin consulté (anesthésiste, etc.) de la pathologie surrénalienne et de son traitement.
4. Surveillance
Elle est surtout clinique +++.
Pour adapter les doses, on se fonde sur la sensation ou non de fatigue (mais non spécifique), sur le poids, la TA (couché et debout). On recherche des signes de surdosage en hydrocortisone (gonflement et rougeur du visage, prise de poids, HTA, etc.) et en fludrocortisone (œdème des membres inférieurs, HTA, etc.), et de sous-dosage (hypotension orthostatique, fatigue, nausées, etc.).
On peut s’aider, pour adapter la dose de fludrocortisone, du dosage de la rénine, l’impression clinique étant toutefois prépondérante. En revanche, il est inutile de mesurer la cortisolémie ou l’ACTH pour adapter la dose d’hydrocortisone (les taux plasmatiques de cortisol seraient très bas avant la prise, reflétant la production endogène, et très hauts pendant quelques heures après la prise du comprimé ; l’ACTH ne se normaliserait qu’en cas de surdosage important).
Biologiquement, il faut vérifier la normalité du ionogramme.