2 - Physiopathologie
La physiopathologie commune du diabète de type 2 est représentée dans la figure 13.4.
L’insulinorésistance se caractérise par :
- l’incapacité de l’insuline à obtenir une réponse maximale au niveau de ses organes cibles ;
- au niveau du muscle lors de la charge en glucose, elle aboutit à un défaut de captation musculaire du glucose ;
- au niveau hépatique, on note un accroissement de la production hépatique de glucose, à l’origine de l’hyperglycémie à jeun.
Il existe également une insulinorésistance adipocytaire.
L’insulinopénie relative est caractérisée par une insuffisance de sécrétion d’insuline, compte tenu du niveau de la glycémie. Ce trouble, qui est présent dès le début de la maladie, est évolutif, inéluctable et s’aggrave avec l’âge et la durée du diabète, jusqu’à conduire au maximum au diabète insulinonécessitant.
2 . 1 - Facteurs génétiques
L’importance des facteurs génétiques peut s’apprécier dans le tableau 13.V.
| Population générale française | 2 à 4 % |
| Jumeaux vrais | 90 à 100 % |
| 2 parents diabétiques | 30 à 60 % |
| 1 apparenté au premier degré | 10 à 30 % |
Plusieurs gènes sont incriminés dans l’apparition d’un diabète de type 2, ces gènes ayant un rôle dans le développement pancréatique ou la synthèse de l’insuline.
2 . 2 - Glucotoxicité
L’hyperglycémie aggrave le déficit de l’insulinosécrétion pancréatique ainsi que l’insulinorésistance, notamment par l’élévation du seuil du « glucose sensor » des cellules bêta.
2 . 3 - Lipotoxicité
La non-freination de la lipolyse en raison de l’insulinopénie et de l’insulinorésistance des adipocytes est responsable d’une augmentation des acides gras libres. Cette augmentation des acides gras libres augmente le « seuil sensor » de l’insulinosécrétion et aggrave la diminution de l’insulinosécrétion. Elle augmente également l’utilisation du glucose stimulée par l’insuline.
2 . 4 - Adipokines
L’insulinorésistance est en partie liée à la sécrétion d’adipokines par les adipocytes comme le TNF.
Définie comme une réponse diminuée à l’administration d’insuline exogène, l’insulinorésistance (figure 13.5) est favorisée par l’obésité androïde, l’âge et la sédentarité.
Elle s’accompagne d’anomalies comme dans le cas du syndrome X (2005), caractérisé par une obésité androïde associée à deux des anomalies suivantes :
- une hypertriglycéridémie ;
- un niveau d’HDLc diminué ;
- une HTA ;
- une hyperglycémie à jeun ou un diabète.
Le profil est à haut risque cardiovasculaire.
Les causes de l’insulinorésistance sont les suivantes :
- non modifiables : la génétique ;
- modifiables :
- la sédentarité -> activité physique ;
- l’excès pondéral -> alimentation équilibrée et adaptée au poids.
Les conséquences de l’insulinorésistance sont un risque vasculaire accru du fait du diabète et des autres anomalies souvent associées : hypertension artérielle (HTA), dyslipidémie, etc.




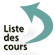

![Fig. 13.5. Insulinorésistance hépatiqueet périphérique (musculaire et adipocytaire) (d’après [7]).](images/figure3.jpg)