5 . 2 - Autosurveillance
Les buts de l’autosurveillance sont :
- de suivre son diabète ;
- d’adapter ses doses ;
- d’avoir une idée de l’équilibre moyen ;
- de gérer les situations d’urgence.
La place de l’autosurveillance urinaire est faible : acétonurie matinale en cas d’hyperglycémie, de troubles digestifs, ou de maladie intercurrente. À noter qu’il est actuellement possible de mesurer les corps cétoniques sur le sang capillaire avec certains appareils.
L’autosurveillance glycémique doit être réalisée au moins 4 fois par jour (préprandial et coucher) et de temps en temps à 3 heures du matin et en postprandial. Les lecteurs portables sont de plus en plus simples et rapides à la condition d’une bonne technique de production de la goutte de sang. Leur exactitude, environ 15 % de variation par rapport à la glycémie de laboratoire, suffit pour l’autocontrôle glycémique par le patient ou les soignants.
Il faut également noter l’utilité d’un carnet de surveillance du diabète bien tenu, et l’utilisation possible de logiciels d’analyse des données.
Les progrès des dispositifs de mesure du glucose sous-cutané en continu permettent actuellement de proposer à certains patients le port d’un tel appareil en ambulatoire, soit en guise de holter glycémique, soit d’outil d’auto-adaptation de l’insulinothérapie.
5 . 3 - Surveillance
1. Hémoglobine glyquée
Fixation non enzymatique (glycation d’une protéine par la réaction de Maillard) et irréversible (réarrangement d’Amadori) du glucose sur toutes les hémoglobines.
Fraction la plus spécifique d’hémoglobine glyquée : HbA1c.
Les méthodes autorisées sont standardisées et certifiées pour donner des résultats similaires à ceux de l’étude DCCT. Il s’agit des méthodes HPLC (high pressure liquid chromatography), immunologiques, avec une valeur normale entre 4 et 6 %.
Le résultat d’HbA1c est habituellement exprimé en unités « NGSP/DCCT », c’est-à-dire en pourcentage de l’hémoglobine totale (mode d’expression des références dans ce chapitre). De nouvelles unités peuvent aussi figurer sur les bons de réponse : les unités « IFCC », exprimées en mmol HbA1c/mol Hb. Un tableau de correspondance entre valeur d’HbA1c et glycémie moyenne peut aussi être fourni à titre indicatif sur la feuille de résultat.
L’objectif pour le diabétique adulte est une valeur d’HbA1c inférieure ou égale à 7 %, tolérance jusqu’à 8 % pour l’enfant de 6 à 12 ans et 8,5 % pour le jeune enfant (< 6 ans). Chez le sujet âgé, l’objectif est à discuter en fonction de l’état clinique.
L’hémoglobine glyquée reflète l’équilibre des 2 à 3 mois précédents (7 % correspondant à une glycémie moyenne de 1,5 g/L ; 9 % correspondant à une glycémie moyenne de 2,1 g/L). Elle est le meilleur indicateur du risque de complications.
Les causes d’erreur de la mesure de l’HbA1c sont : anémie hémolytique, urémie, hémoglobinopathie, traitement par EPO, saignées. Dans ces cas, le dosage de fructosaminémie peut avoir un intérêt.
2. Autres éléments de surveillance
Consultation spécialisée au moins 3 à 4 fois par an et surveillance des éléments suivants :
- profil lipidique, créatinine, microalbuminurie, ECBU et ECG (une fois par an) ;
- examen ophtalmologique (FO ou rétinographie par caméra non mydriatique) au moins une fois par an pour ce qui est du dépistage. Dès qu’il y a des lésions de rétinopathie diabétique, la prise en charge par l’ophtalmologiste peut être plus rapprochée.
5 . 4 - Traitement insulinique
Le traitement principal du diabète de type 1 est un traitement à vie, palliatif.
1. Variétés d’insuline
a. Insuline recombinante
L’insuline humaine recombinante est strictement identique à l’insuline humaine.
b. Analogues de l’insuline
Les analogues de l’insuline sont structurellement modifiés pour obtenir des propriétés pharmacodynamiques intéressantes. Les analogues rapides sont obtenus en modifiant la partie de la molécule participant à la formation des hexamères d’insuline. Les analogues lents sont obtenus soit en modifiant le point isoélectrique de la molécule (Lantus®, insuline parfaitement soluble à pH acide et précipitant au pH physiologique pour former un dépôt sous-cutané à libération lente), soit en formant un analogue acylé (adjonction d’un acide gras à courte chaîne), susceptible d’être adsorbé par l’albumine et ralenti dans sa solubilisation (Levemir®). Les analogues rapides ont l’avantage d’être rapidement actifs au moment de la prise alimentaire et de ne pas persister pendant la phase interprandiale. Ils seront injectés juste avant de passer à table. Les analogues lents ont une action prolongée, sans pic d’activité, et relativement reproductible d’un jour à l’autre. Ils seront administrés en 1 ou 2 injections à heure fixe. Ces analogues sont toujours concentrés à 100 U/mL.
Il existe donc une gamme de produits qui diffèrent par leur durée d’action :
- les analogues rapides (3 à 5 heures : Humalog®, Novorapid®, Apidra®) ;
- les insulines humaines rapides (4 à 8 heures : Actrapid®, Umuline rapide®ou Insuman® ) qui couvrent les besoins prandiaux ;
- les insulines humaines ralenties par la protamine, d’action intermédiaire (9 à 16 heures : NPH, pour Neutral Protamine Hagedorn), ou par un excès de zinc, d’action prolongée (environ 24 heures : Ultraltard®) ;
- et les analogues lents (20 à 24 heures : Lantus®, 12 à 24 heures : Levemir®), qui couvrent les besoins basaux.
Il existe aussi des mélanges préconditionnés d’analogues rapides et d’analogues ralentis par la protamine (Humalog Mix®25 ou 50, Novomix®30, 50 et 70), dont le numéro correspond à la proportion d’analogue rapide présent dans le mélange.
2. Facteurs de résorption sous-cutanée
Ces facteurs de résorption sont :
- la profondeur ;
- la zone ;
- la dose (variation intra-individuelle de 15 à 50 %) ;
- l’environnement thermique ;
- l’activité musculaire au niveau du membre où a été réalisée l’injection (la vasodilatation accélère le passage de l’insuline dans le sang).
3. Vecteurs
Les vecteurs sont de deux types :
- les stylos à insuline réutilisables ou jetables pour toutes les insulines solubles, plus pratiques que les seringues jetables ;
- les pompes portables pour l’administration continue, modulée et sous-cutanée d’insuline humaine, ou mieux d’analogue rapide. Plus efficaces, plus flexibles mais plus contraignantes et plus chères que le traitement basal – bolus par injections multiples ; à réserver aux échecs de l’insulinothérapie optimisée.
4. Schémas
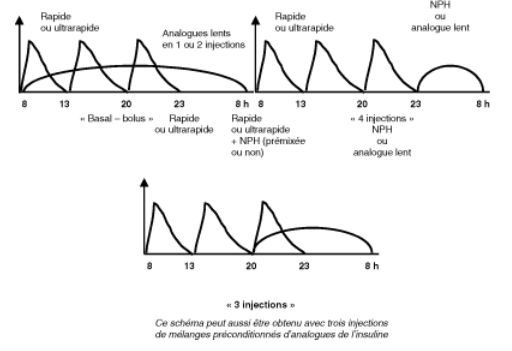
Ces schémas, représentés dans la figure 13.2, sont à choisir suivant l’acceptation, l’autonomisation du patient et les objectifs thérapeutiques. Actuellement, le traitement le plus utilisé est un schéma type basal ? bolus utilisant les analogues lents en 1 ou 2 injections pour assurer l’insulinisation basale ? et des injections prandiales d’analogues rapides pour assurer la métabolisation des repas. Ce schéma à 4 ou 5 injections quotidiennes est bien accepté parce qu’il limite le risque d’hypoglycémie et permet de moduler l’insulinothérapie aux diverses circonstances de la vie (possibilité de retarder l’heure ou de sauter un repas, grasse matinée, etc.).
5. Doses
En général, moins de 1 U/kg de poids, auto-adaptation en fonction des glycémies (rétrospective ±instantanée), de l’activité physique et de l’alimentation prévues.
Une méthode personnalisée dite « insulinothérapie fonctionnelle » est développée dans de nombreux centres. Elle vise à éduquer le patient diabétique pour qu’il puisse adapter son insulinothérapie à son mode de vie. Elle est fondée sur une étude analytique des raisonnements d’adaptation des doses d’insuline, distinguant :
- l’insuline pour vivre (basale) ;
- l’insuline pour manger (schématiquement fondée sur un ratio d’unités d’insuline par unité alimentaire de 10 g de glucides) ;
- l’insuline pour traiter (l’adaptation de l’insuline rapide pour corriger une hypo ou une hyperglycémie) ;
- l’insuline pour l’activité physique et autres situations de vie.
Cette méthode vise à conférer plus d’autonomie et à libérer le patient de certaines contraintes qui retentissent défavorablement sur la qualité de vie.
6. Effets secondaires de l’insulinothérapie
Les effets secondaires sont les suivants :
- hypoglycémies (cf. chapitre 11 : « Hypoglycémie ») ;
- prise de poids (+ 5 kg dans l’essai DCCT) ; l’optimisation du contrôle glycémique a tendance à faire prendre du poids (augmentation de la masse maigre, suppression de la glycosurie, resucrage des hypoglycémies) ;
- allergie rarissime ;
- lipoatrophies d’origine immunologique ;
- lipohypertrophies si piqûres au même endroit.
5 . 5 - Traitement non insulinique
Accompagnement et soutien psychologique comme pour toute maladie chronique.
Alimentation variée et sans interdits, mais horaires et apports glucidiques réguliers (notion d’équivalence, d’index glycémique, de collations même si celles-ci sont moins de mise avec les analogues rapides, cf. infra).
Exercice physique à recommander et à prendre en compte pour les doses d’insuline ; risque d’hypoglycémie (cf. infra).
Utilité des associations de patients (AFD : Association française des diabétiques, AJD : Aide aux jeunes diabétiques) pour le soutien psychologique et comme sources d’information, d’activités de groupe, de défense des intérêts communs auprès des pouvoirs publics, des compagnies d’assurances, etc.
5 . 6 - Voies d’avenir
Parmi les voies d’avenir, nous proposons des notions générales à travers les points suivants :
- amélioration des capteurs de glycémie : implantabilité, lecture directe, lien au matériel d’injection, etc. ;
- insuline inhalée ou autres voies d’administration : orale, patch percutané ;
- nouveaux analogues de très longue durée d’action ;
- pompes « patch » jetables ;
- pompes implantables plus ou moins rétrocontrôlées (pancréas artificiel) ;
- greffes de pancréas (cette dernière est déjà la règle, sauf contre-indication chez le diabétique néphropathe) et d’îlots ;
- développement des programmes de transplantation de cellules souches ;
- prévention : immunothérapie, vaccination des sujets à risque ;
- action permettant la régénération des cellules bêta.