2
-
Hérédité autosomique dominante
2
.
1
-
Définition
Les gènes responsables des maladies transmises sur le mode autosomique dominant (AD) sont localisés sur les autosomes.
L'allèle muté responsable de la maladie est dominant sur l'allèle ‘sauvage’: la maladie s'exprime chez les hétérozygotes.
En pathologie humaine, les situations où l'on observe des homozygotes pour des allèles mutés responsables de pathologies dominantes sont très rares; cette situation peut conduire à un phénotype identique ou plus sévère.
2
.
2
-
Caractéristiques généalogiques des maladies AD
- Les deux sexes sont atteints avec la même fréquence.
- La transmission de la maladie peut se faire par les deux sexes.
- Les transmissions père-fils sont pathognomoniques de l'hérédité AD.
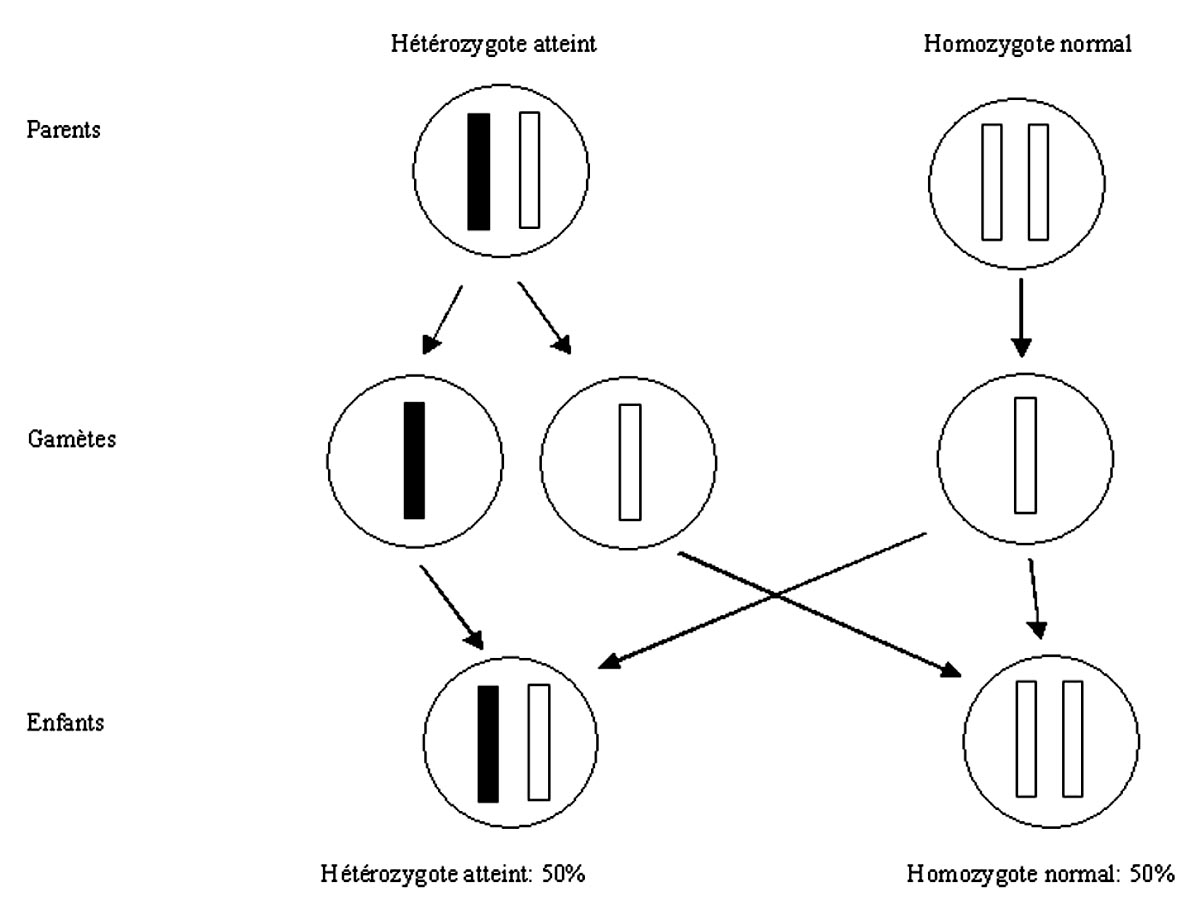
- Tout sujet porteur d'un allèle morbide AD a un risque de 50% (1/2) de le transmettre à ses enfants quelque soit leur sexe. (figure 2).
- Les sujets atteints se retrouvent sur plusieurs générations et leur répartition apparaît verticale sur l'arbre généalogique.
2
.
3
-
Exemples de maladie AD
- Hypercholestérolémie familiale : maladie due à une anomalie du gène du récepteur pour le LDL cholestérol (19p13)
- Achondroplasie : nanisme dû à une mutation dans le gène FGFR3 (4p16.3).
- Maladie de Marfan: affection touchant notamment le squelette, l'oeil, les gros vaisseaux et due à des mutations dans le gène de la fibrilline 1 (15q21).
- Chorée de Huntington: maladie neurologique dégénérative de l'adulte (4p16).
- Ostéogenèse imparfaite: maladie avec fragilité osseuse due à une anomalie du collagène de type I.
- Neurofibromatose de type I (NF1): maladie pouvant associer de façon très variable des signes cutanés, des tumeurs nerveuses, des signes osseux, des difficultés d’apprentissage (17q11).
- Certaines prédispositions pour les cancers se transmettent comme des caractères dominants; c'est le cas, par exemple, de 10% des cancers du sein, de certains cancers du colon, des formes familiales de cancers médullaires de la thyroïde et des formes familiales de rétinoblastome (cancer de la rétine de l'enfant).
2
.
4
-
Particularités de l'hérédité AD
2
.
4
.
1
-
Pénétrance incomplète
- Dans certaines maladies, les individus porteurs de la mutation peuvent ne présenter aucun signe de l'affection ; on parle alors de pénétrance incomplète du gène morbide. Dans ce cas, un sujet apparemment sain peut être porteur du gène muté et transmettre la maladie à sa descendance.
- La pénétrance d'un allèle morbide est définie par le rapport suivant : nombre d'hétérozygotes malades / nombre total d'hétérozygotes.
En pratique, une pénétrance de 80% signifie qu’un sujet porteur de la mutation a 80% de risque d'être malade.
Ce phénomène est expliqué par l'interaction de l'allèle morbide avec des gènes modificateurs et/ou des facteurs de l'environnement.
- La pénétrance d'un gène peut aussi varier en fonction d'autres paramètres: l'âge (par ex: la pénétrance du gène responsable de la chorée de Huntington est de 0 à la naissance, de 50% vers 40 ans et de 100% vers 70 ans) ou le sexe.
2
.
4
.
2
-
Expressivité variable
Un allèle morbide peut s’exprimer par des signes cliniques différents d'un individu à l'autre. C’est le cas, par exemple, de la neurofibromatose de type I dont les signes peuvent varier chez les membres d'une même famille.
2
.
4
.
3
-
Néomutations ou mutations de novo
Il arrive qu'un sujet malade naisse de deux parents non porteurs de la mutation.
Ce phénomène est expliqué par l'apparition de l'allèle muté dans l'un des gamètes parentaux; il s'agit d'une mutation de novo ou néomutation. Dans la descendance du sujet porteur de cette nouvelle mutation, on retrouve les caractéristiques de transmission de l'hérédité AD. Pour certaines maladies, la proportion de néomutations est très élevée; c'est le cas, par exemple, de l'achondroplasie (80%), de la NF1 (50%) et de la maladie de Marfan (50%). Ces néomutations sont favorisées par l’âge paternel élevé.
2
.
4
.
4
-
Mosaïques germinales
Le mosaïcisme germinal est défini par la présence d'une double population de gamètes, certains étant porteurs de l’allèle muté, d'autres de l’allèle sauvage.
Le parent porteur d'une mutation germinale en mosaïque peut la transmettre à sa descendance. Si cette mutation est absente de ses cellules somatiques, la maladie ne s'exprimera pas du tout chez lui.
Ce concept est d'une grande importance pour le conseil génétique puisqu'il signifie que des personnes, non porteuses en apparence de la mutation, peuvent avoir plusieurs enfants atteints.
Le mosaïcisme germinal a été décrit dans diverses affections dominantes (ex: la NF1 ou l’ostéogénèse imparfaite) ou liées au chromosome X (ex: la dystrophie musculaire de Duchenne).
2
.
5
-
Mécanismes de la dominance
-
Mutations avec perte de fonction ou haplo-insuffisance
Un seul allèle fonctionne sur les deux, mais la quantité de protéine est insuffisante pour assurer une fonction normale.
Exemple : dans l'hypercholestérolémie familiale, la présence de la moitié des récepteurs LDL ne suffit pas pour obtenir un taux circulant normal de LDL cholestérol.
-
Mutation avec gain de fonction
Dans ce type de mutation, la protéine issue de l'allèle muté fonctionne différemment de la protéine physiologique. Cette fonction peut être amplifiée, dérégulée, toxique pour la cellule ou encore complètement nouvelle.
-
Mutation dominante négative
Dans ce type de mutation, le produit de l'allèle muté interfère avec la fonction de la protéine normale.
C'est par exemple le cas dans l'ostéogenèse imparfaite où la formation du collagène de type I qui est une protéine multimèrique (assemblage de 3 molécules) est fragilisée par la présence d'une molécule anormale.
2/4