3 - Facteurs de risque
A. Helicobacter pylori (H. pylori)
H. pylori est un bacille à gram négatif à transmission oro-fécale. Il a été reconnu comme facteur étiologique de cancer gastrique (adénocarcinome et lymphome) en 1994 par l’OMS.
La gastrite (inflammation de la muqueuse), induite par H. pylori, peut évoluer vers la gastrite chronique atrophique, la métaplasie puis la dysplasie et le cancer. L’adénocarcinome distal de type intestinal fait suite à l’évolution de cette gastrite chronique.
Toutefois, moins de 1 % des patients infectés par H. pylori développeront un cancer gastrique. L’infection à H. pylori n’est donc pas suffisante à elle seule pour induire un cancer, mais elle intervient à un stade précoce de la cancérogenèse, associée à d’autres facteurs de risque.
Le fait de ne pas mettre en évidence H. pylori sur les biopsies gastriques lors du diagnostic de cancer ne signifie pas que l’infection n’est pas en cause dans la genèse de celui-ci, car la bactérie a pu être éliminée de l’estomac (l’atrophie et l’achlorhydrie secondaires à l’infection sont peu propices à la survie de la bactérie). La recherche de l’infection par une sérologie peut être utile.
B. Facteurs génétiques
La recherche de prédispositions familiales est recommandée (antécédents familiaux, survenue avant 40 ans) afin de poser l’indication d’une consultation d’oncogénétique.
1. Adénocarcinomes gastriques diffus héréditaires
Les cancers gastriques diffus héréditaires sont dus à une mutation germinale du gène CDH1 à transmission autosomique dominante, responsable de la perte de fonction de la protéine E-Cadhérine.
Le diagnostic doit être évoqué quand, dans une même famille et sur au moins deux générations successives, il existe 2 cas, si l’un des cancers gastriques est découvert avant 50 ans, ou 3 cas indépendamment de l’âge de découverte. En cas de suspicion d’une forme héréditaire, le patient sera adressé en consultation d’oncogénétique.
2. Adénocarcinomes gastriques survenant dans le cadre de syndromes familiaux
Le risque de cancer gastrique est augmenté chez :
– les apparentés au premier degré de malades ayant un cancer de l’estomac ;
– les patients ayant un syndrome (
HNPCC
, cancer colorectal non polyposique familial (voir chapitre 9)) ou syndrome de Lynch ;
– les patients atteints de polypose adénomateuse familiale (PAF (voir chapitre 9)).
Même si le risque de cancer gastrique n’est pas au premier plan, il est recommandé dans ces 3 situations de chercher systématiquement H. pylori (le plus souvent lors d’une endoscopie digestive haute) et de l’éradiquer s’il est présent.
C. Facteurs environnementaux
Les facteurs les mieux établis exposant au risque d’adénocarcinome gastrique sont :
– le tabagisme ;
– la consommation élevée de sel ;
– le niveau socio-économique bas ;
– la faible consommation de fruits et légumes.
L’interaction entre ces facteurs et l’infection par H. pylori est probable.
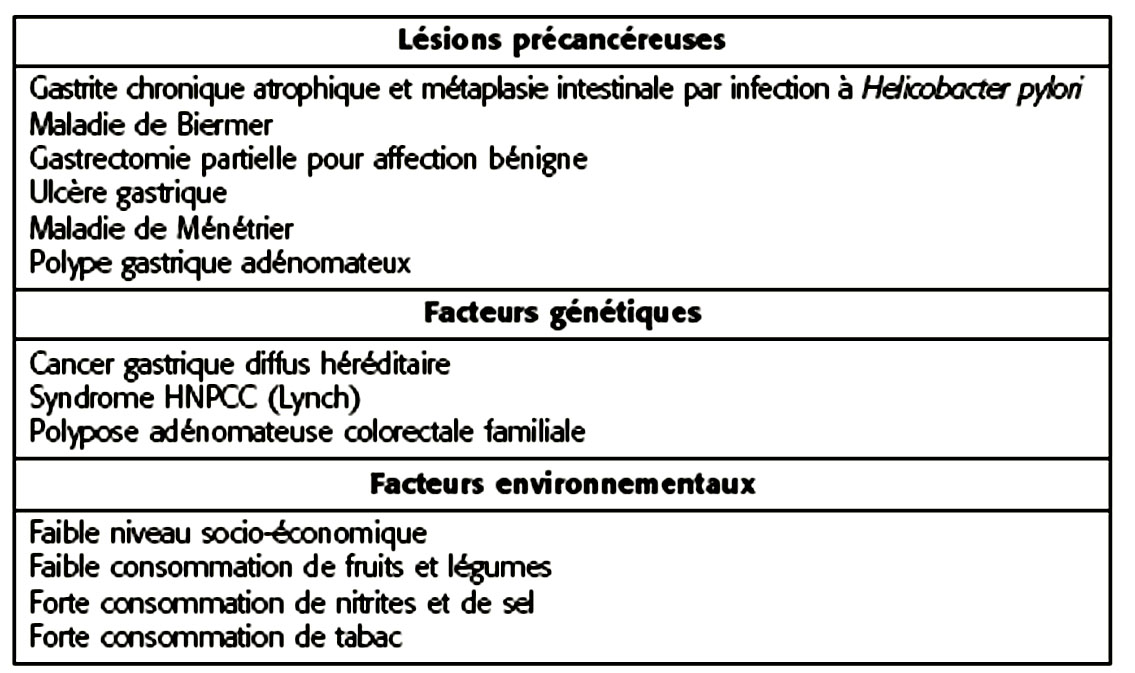
D. Lésions précancéreuses
Les principales conditions précancéreuses à l’origine des cancers gastriques sont indiquées dans le tableau 10.I.
La maladie de Biermer (gastrite atrophique fundique auto-immune) peut aussi favoriser la survenue de tumeurs endocrines gastriques.
Le risque d’adénocarcinome sur moignon gastrique après gastrectomie partielle n’est significatif qu’après 15 ans (rôle probable du reflux biliaire).
Une endoscopie de contrôle à la fin de tout traitement (6 à 8 semaines) pour ulcère gastrique doit être réalisée, afin de faire de nouvelles biopsies sur la cicatrice ou les berges pour ne pas méconnaître un cancer.
L’ulcère duodénal n’est pas à risque de dégénérescence et ne nécessite donc pas de contrôle endoscopique.