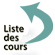Introduction
Inflammation aiguë des feuillets péricardiques, la péricardite aiguë pose des problèmes de difficultés du diagnostic, expose au risque de tamponnade et pour certaines étiologies au risque d’évolution vers la constriction.
1 - Diagnostic d'une péricardite aiguë
Le diagnostic de péricardite aiguë est évoqué devant l’association d’une douleur thoracique évocatrice, d’un éventuel frottement péricardique, de modifications ECG typiques et d’un épanchement péricardique. La présence de deux de ces critères est nécessaire pour confirmer le diagnostic. La réalisation d’un ECG et d’une échocardiographie est donc systématique.
1 . 1 - Signes cliniques
- Fièvre modérée, présente d’emblée, associée à des myalgies, à une asthénie, souvent précédée d’un épisode grippal. La fièvre est moins fréquente chez le sujet âgé.
- Douleur thoracique, rétrosternale ou précordiale gauche, prolongée, résistante à la trinitrine, majorée en décubitus à l’inspiration profonde et à la toux, calmée par la position assise penchée en avant (antéflexion).
- Dyspnée parfois associée – également soulagée par la position assise penchée en avant – ou toux sèche, dysphonie et hoquet également possibles.
- Frottement péricardique précoce, râpeux, systolodiastolique, variant dans le temps et les positions, crissement de cuir neuf ou froissement de soie, confirme le diagnostic mais inconstant et fugace. Il s’accompagne d’une tachycardie. Son absence n’élimine pas le diagnostic.
- Épanchement pleural parfois présent.
1 . 2 - Examens complémentaires
1. ECG
Cf. item 309.
À répéter, peut être normal.
Anomalies diffuses non systématisées sans image en miroir évoluant en quatre stades :
- stade I : sus-décalage ST concave vers le haut, ondes T positives le premier jour ;
- stade II : ondes T plates entre la 24e et la 48e heure ;
- stade III : ondes T négatives la première semaine ;
- stade IV : normalisation au cours du premier mois.
Les autres signes sont :
- sous-décalage de PQ présent à la phase initiale ;
- tachycardie sinusale, extrasystole atriale, fibrillation atriale, flutter atrial ;
- microvoltage si épanchement abondant (amplitude QRS < 5 mm et < 10 mm respectivement dans les dérivations périphériques et précordiales).
2. Bilan biologique initial
Le bilan biologique initial doit être limité en l’absence d’orientation clinique, de signes de gravité ou de récidive :
- marqueurs inflammatoires : NFS, VS, CRP ;
- marqueurs de la nécrose : troponines I ou T ou CPK-MB, leur augmentation significative, éventuellement coexistant avec un trouble de cinétique ventriculaire gauche global ou segmentaire, oriente vers une myocardite associée ;
- ionogramme sanguin, urée, créatinine ;
- hémocultures si fièvre, discuter IDR.
3. Radiographie thoracique
- Normale le plus souvent.
- Rectitude du bord gauche ou cardiomégalie avec cœur triangulaire en carafe si épanchement abondant.
- Aide au diagnostic étiologique, notamment en cas de pathologie pulmonaire associée ou d’épanchement pleural.
4. Échocardiographie
Parfois normale.
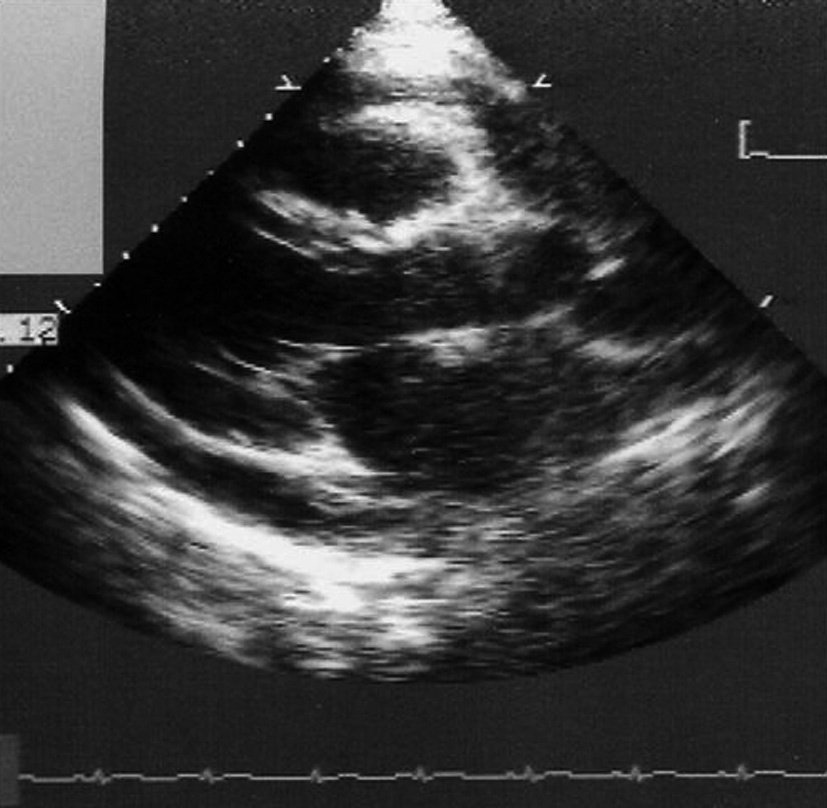
Epanchement péricardique : sur l’existence d’un simple décollement des deux feuillets péricardiques ou d’un épanchement péricardique qui apparaît sous la forme d’un espace clair vide d’écho (figure 1). L’échocardiographie apprécie l’abondance, la topographie et la tolérance hémodynamique de l’épanchement péricardique et confirme le diagnostic d’une éventuelle tamponnade.
Masse péricardique : l’échocardiographie permet de visualiser une éventuelle masse localisée dans la cavité péricardique, métastases ou caillots dans le cadre d’une péricardite néoplasique. Des bandes de fibrine aboutissant à un épanchement péricardique cloisonné sont facilement identifiées par l’échographie.
5. Autres examens complémentaires parfois utiles en seconde intention
Le scanner thoracique et l’IRM cardiaque sont parfois utiles en deuxième intention lorsque le patient n’est pas échogène ou en présence d’une péricardite néoplasique ou d’un épanchement péricardique cloisonné. L’IRM a l’avantage de visualiser la cavité péricardique sans injection de produit de contraste ni irradiation.
La ponction péricardique est à envisager en cas de tamponnade, de forte suspicion de péricardite néoplasique, et en présence d’un épanchement péricardique abondant, symptomatique, malgré un traitement médical bien conduit depuis une semaine.
Les analyses réalisées sur les prélèvements du liquide péricardique sont :
- glucose, protides, lactate déshydrogénase ;
- cytologie et analyse microscopique (colorations de Gram et de Ziehl-Nielsen) ;
- mise en culture bactérienne ;
- techniques de PCR (recherche virale et tuberculose).
Un drainage péricardique chirurgical est à privilégier en cas de suspicion de péricardite aiguë purulente. Le liquide péricardique est recueilli pour analyse cytologique et microbiologique.
6. Faut-il hospitaliser le patient ?
Une fois le diagnostic établi, l’hospitalisation ne doit pas être systématique. Elle est utile pour réaliser l’enquête étiologique, dépister une éventuelle complication et débuter le traitement.
- Hospitalisation en cas de tableau clinique orientant vers une étiologie.
- Hospitalisation en cas de facteurs prédictifs de tamponnade :
- fièvre supérieure à 38 ?C ;
- symptômes présents depuis plusieurs semaines ;
- patient immunodéprimé ;
- patient sous AVK ;
- après un traumatisme thoracique ;
- présence d’une myocardite associée ;
- épanchement péricardique abondant (> 20 mm) ou tamponnade ;
- résistance au traitement anti-inflammatoire (aspirine ou AINS) prescrit depuis 7 jours.
1 . 3 - Etiologies
Dans neuf cas sur dix, la cause est virale ou inconnue (péricardite aiguë idiopathique).
1. Péricardite aiguë virale
Étiologie la plus fréquente, mais rarement prouvée, liée à l’infection virale et à la réaction immune associée.
Le tableau clinique typique est :
- sujet jeune, syndrome grippal récent, prédominance masculine ;
- début brutal, fébrile ;
- douleur thoracique typique augmentant à l’inspiration, frottement péricardique ;
- modifications ECG typiques ;
- échocardiographie normale le plus souvent ;
- épanchement pleural souvent associé.
Les virus en cause sont nombreux : entérovirus (coxsackies A et B), échovirus, adénovirus, cytomégalovirus, parvovirus B19, Epstein-Barr, herpès, VIH, hépatite C, influenza…
Les sérologies répétées à 15 jours d’intervalle peuvent mettre en évidence une élévation des anticorps spécifiques, orientant vers le diagnostic de péricardite virale, mais seul le diagnostic viral (techniques de PCR à partir de l’épanchement péricardique ou d’une biopsie du péricarde) confirme le diagnostic. Il est cependant inutile dans les formes typiques sans gravité.
L’évolution est le plus souvent favorable. Le taux de récidive est cependant important allant de 30 à 50 %. La survenue d’une tamponnade ou l’évolution vers une constriction péricardique reste rare. Dans certaines formes de péricardite chronique récidivante, après diagnostic viral, la prescription de traitements spécifiques (immunoglobulines, interféron α) est discutée.
Au cours de l’infection VIH, la survenue d’une péricardite avec épanchement péricardique est fréquente. Les mécanismes sont multiples ; la péricardite peut être liée à :
- l’infection virale par le VIH ou d’autres virus ;
- une surinfection bactérienne ou fungique chez un patient immunodéprimé ;
- la présence d’un lymphome ou d’un sarcome de Kaposi.
2. Péricardite purulente
Elle est rare mais grave.
Les germes sont : staphylocoques, pneumocoques, streptocoques, bacilles Gram négatif…
Ces péricardites, en nette diminution, touchent essentiellement les sujets immunodéprimés ou porteurs d’infection sévère (septicémie, affection pleuropulmonaire, après chirurgie cardiaque ou thoracique).
Le pronostic est sévère avec survenue fréquente d’une tamponnade ou évolution vers la constriction péricardique.
Le traitement repose sur une antibiothérapie adaptée au germe retrouvé dans le liquide péricardique (ponction péricardique). Le drainage chirurgical est souvent nécessaire.
3. Péricardite tuberculeuse
Il s’agit d’une péricardite subaiguë liquidienne avec altération de l’état général et fièvre modérée persistante, le plus souvent chez :
- un sujet tuberculeux, âgé ou greffé ;
- un patient infecté par le VIH ;
- un patient alcoolique.
Une notion de tuberculose est retrouvé dans l’entourage ou un virage récent de l’IDR est observé (faussement négatif dans près d’un tiers des cas).
Les anomalies pulmonaires radiologiques sont fréquentes.
Recherche du BK (Mycobacterium tuberculosis), techniques de PCR (expectoration, liquide pleural et péricardique, tubages gastriques), fortes concentrations d’adénosine déaminase dans le liquide de ponction péricardique. Parfois, une ponction biopsie du péricarde met en évidence un granulome inflammatoire.
L’évolution est fréquente vers une tamponnade, une récidive ou une constriction péricardique.
Le traitement repose sur le traitement antituberculeux associé pour certains aux corticoïdes (prednisone) afin de diminuer le risque d’évolution vers une constriction péricardique.
4. Péricardite néoplasique
Les tumeurs primitives du péricarde (mésothéliome péricardique primitif) sont rares, 40 fois moins fréquentes que les métastases. Les tumeurs secondaires les plus fréquentes sont : cancer bronchique, cancer du sein, mélanomes, leucémies, lymphomes, sarcome de Kaposi (SIDA).
L’épanchement péricardique hémorragique est fréquent, de même que la survenue d’une tamponnade.
Le diagnostic est confirmé par l’échocardiographie, parfois complétée par un scanner ou une IRM cardiaque.
L’analyse du liquide de ponction péricardique ou la réalisation d’une biopsie péricardique sont essentielles au diagnostic de malignité.
En cas de tamponnade, la ponction péricardique en urgence s’impose.
La récidive de l’épanchement péricardique est fréquente et impose un suivi clinique et échocardiographique.
5. Péricardite au cours des maladies systémiques auto-immunes
Les étiologies les plus fréquentes sont lupus, polyarthrite rhumatoïde, sclérodermie, périartérite noueuse, dermatomyosite.
Les péricardites auto-immunes sont également fréquentes, mais restent un diagnostic d’élimination. Les critères diagnostiques à retenir sont : augmentation des lymphocytes, présence d’anticorps anti-sarcolemme dans le liquide péricardique, myocardite associée.
6. Péricardite et infarctus du myocarde
La péricardite précoce (J3 – J5) est d’évolution le plus souvent favorable, elle survient au décours d’un infarctus transmural.
La péricardite tardive (2–16e semaine) correspond au syndrome de Dressler, elle associe fièvre, péricardite, pleurésie, arthralgies, altération de l’état général, syndrome inflammatoire important, allongement de l’espace QT à l’ECG. Ce syndrome est devenu rare depuis la reperfusion coronaire précoce.
7. Péricardite et insuffisance rénale chronique
Il faut distinguer la péricardite urémique survenant chez des insuffisants rénaux sévères non encore dialysés ou dans les premières semaines suivant la mise en route de la dialyse et la péricardite chez le patient dialysé au long cours, témoignant le plus souvent d’un traitement épurateur inadapté.
8. Syndrome post-péricardiotomie
Le syndrome post-péricardiotomie, d’origine immunologique, survient dans les jours ou mois suivant une chirurgie cardiaque ou après transplantation cardiaque.
La survenue d’une tamponnade est possible et la chirurgie cardiaque représente actuellement la première cause de constriction péricardique.
9. Causes plus rares
- Dissection aortique avec tamponnade.
- Irradiation thoracique, en général 1 an après.
- Traumatismes thoraciques ou cardiaques. Au cours des cathétérismes, notamment après ablation d’une arythmie par radiofréquence, après pose d’un stimulateur cardiaque ou en postopératoire immédiat.
- Certains médicaments (hydralazine, pénicilline).
- Hypothyroïdie.
- Rhumatisme articulaire aigu.