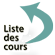4
-
Athérosclérose
L’athérosclérose est une association variable de remaniements de l’intima des artères de gros et moyen calibre, consistant en une accumulation focale de lipides, de glucides complexes, de sang et de produits sanguins, de tissus fibreux et de dépôts calciques, le tout s’accompagnant de modifications de la média (définition de l’OMS de 1957).
L’athérosclérose est une maladie extrêmement fréquente, notamment dans les pays industrialisés, dont les répercussions cliniques sont très variables (infarctus du myocarde, accident vasculaire cérébral, embolie, thrombose, etc.) : il s’agit donc d’un problème majeur de santé publique.
N.B. : étymologie de l’athérosclérose = athérome + sclérose. L’athérome (du grec athere : bouillie) désigne la partie lipidique ; la sclérose (du grec scleros : dur) est un terme macroscopique ancien désignant la fibrose (voir chapitre 3).
Rappel histologique : une artère est constituée de trois tuniques : l’intima (endothélium et zone sous-endothéliale), séparée par la limitante élastique interne de la média (tunique épaisse constituée de cellules musculaires lisses et de fibres élastiques) et l’adventice (figure 4.16).
4
.
1
-
Épidémiologie
Les facteurs de risque de l’athérosclérose sont :
L’âge : l’athérosclérose est la plus commune des maladies artérielles et l’une des principales causes de décès au-delà de 40 ans dans les pays industrialisés. En fait, cette affection peut débuter très précocement dès les premiers mois de la vie et évoluer insidieusement, si bien qu’avec le vieillissement, tous les individus sont porteurs de lésions athéroscléreuses, mais avec une extension et une sévérité extrêmement variables de l’un à l’autre.
Le sexe : l’homme est plus touché que la femme. Les lésions s’aggravent chez la femme après la ménopause.
L’alimentation : alimentation riche en graisses animales et en protéines.
Le mode de vie : surmenage et stress ; tabagisme ; sédentarité.
Facteurs métaboliques et maladies associées : diabète, hypertension, obésité, hypothyroïdie primitive (myxœdème), hyperlipoprotéinémies.
Facteur génétique : le risque d’infarctus du myocarde est 5 fois plus élevé que pour l’ensemble de la population si le père ou la mère a précocement souffert d’athérosclérose coronarienne.
4
.
2
-
Formes topographiques
Les lésions siègent sur l’aorte et sur les grosses et moyennes artères (carotides internes, coronaires, sous-clavières, artères rénales, etc.) et prédominent plus particulièrement dans les zones de turbulence : bifurcations, coudures, naissance des collatérales (ostia) et segments d’artère « fixés » au squelette (ex : l’aorte sous-diaphragmatique).
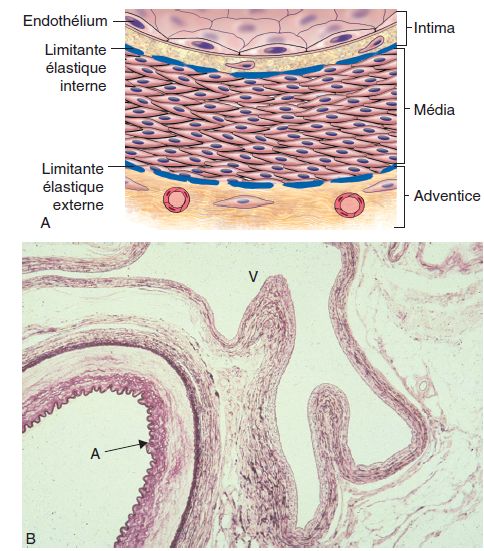
Sur l’aorte : le segment abdominal sous-diaphragmatique est le plus touché notamment au niveau du carrefour aortique. Sur l’aorte thoracique, le segment ascendant et le sommet de la crosse sont surtout intéressés (figure 4.17).
Sur les artères cervico-céphaliques : les lésions touchent les artères carotides et vertébrales, dans leur trajet cervical et intracrânien.
Au niveau des viscères : les lésions se développent sur les premiers centimètres du vaisseau (coronaires, artères rénales, artères mésentériques, etc.) (figure 4.18).
Au niveau des membres : les lésions atteignent surtout les membres inférieurs et peuvent s’étendre jusqu’à mi-jambe. L’atteinte des membres supérieurs est rare.
Au niveau des artères pulmonaires : il n’existe des lésions d’athérosclérose qu’en cas d’hypertension artérielle pulmonaire associée.
Remarque
Il n’existe jamais d’athérosclérose sur les segments veineux sauf sur les greffons veineux (utilisés pour remplacer un segment artériel lésé) après un phénomène pathologique appelé « artérialisation veineuse ». Ces lésions sont également notées en cas d’hyperpression sur les segments veineux : fistules congénitales ou acquises.
4
.
3
-
Formes anatomopathologiques
Classifications macroscopique et histologique des lésions de l’athérosclérose
Sur le plan macroscopique, l’OMS propose les quatre grades suivants :
- grade I : stade débutant constitué surtout de stries lipidiques ;
- grade II : stade moyen comportant des plaques athéroscléreuses non compliquées ;
- grade III : plaques ulcérées et nécrosées avec hémorragies ;
- grade IV : plaques massivement calcifiées et ulcérées.
Sur le plan histologique, l’American heart association (AHA) a proposé dès 1995 les types évolutifs ci-dessous :
- lésions précoces :
- type I : présence de quelques macrophages spumeux sous-endothéliaux visibles en microscopie (dans l’intima),
- type II : strie lipidique (visible macroscopiquement) correspondant à des amas d’histiocytes spumeux dans l’intima, plus nombreux que précédemment ;
- lésions intermédiaires :
- type III : accumulation de lipides extra-cellulaires en faible quantité ;
- lésions avancées :
- type IV : apparition d’un centre lipidique, avec cristaux de cholestérol, sans fibrose,
- type V : plaque athéroscléreuse fibro-lipidique classique,
- type VI : plaque athéroscléreuse compliquée (VIa : ulcération, VIb : hémorragie, VIc : thrombose).
Ces formes sont décrites ci-après en suivant l’histoire naturelle des lésions. Certaines lésions initiales peuvent régresser tandis que d’autres progresseront vers des lésions constituées.
4
.
3
.
1
-
Lésions initiales de la maladie
Point et strie lipidique
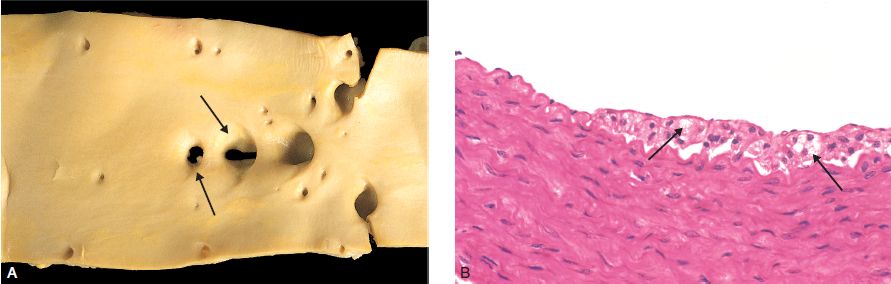
Macroscopie : le point lipidique est une élevure jaunâtre inférieure à 1 mm ; la strie lipidique est une fine traînée jaunâtre à peine saillante, allongée dans le sens du courant sanguin, mesurant quelques millimètres. Ces stries peuvent s’anastomoser, prenant un aspect « réticulé ».
Microscopie : le point et la strie sont formés par des amas de cellules lipophagiques, situées dans l’intima (il s’agit surtout de macrophages et plus rarement de myocytes dédifférenciés en myofibroblastes qui se chargent de graisses). Ces lipophages correspondent à des cellules spumeuses, à cytoplasme clair, surchargé de cholestérol (figure 4.19).
Ces lésions peuvent s’observer avant l’âge d’un an et culminent en extension et incidence à l’adolescence. Elles peuvent soit régresser et disparaître, soit évoluer progressivement vers les autres lésions de l’athérosclérose. Elles n’entraînent aucune manifestation clinique.
Plaque gélatineuse
Macroscopie : plaque grisâtre et translucide sur l’intima, de 0,5 à 1 cm de diamètre.
Microscopie : œdème sous-endothélial (riche en chondroïtine et héparane sulfate, mais dépourvu de lipides).
Ces lésions sont dues à un « insudat », c’est-à-dire au passage de plasma sous l’endothélium par augmentation de la perméabilité endothéliale.
Ces lésions peuvent régresser, se transformer en plaque fibreuse ou bien se charger en lipides et se transformer en plaque d’athérosclérose.
4
.
3
.
2
-
La lésion constituée de la maladie : la plaque d’athérosclérose
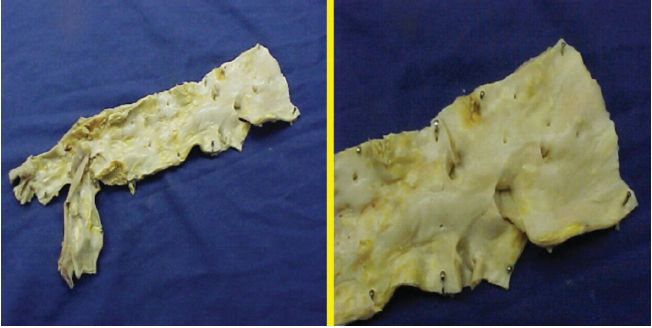
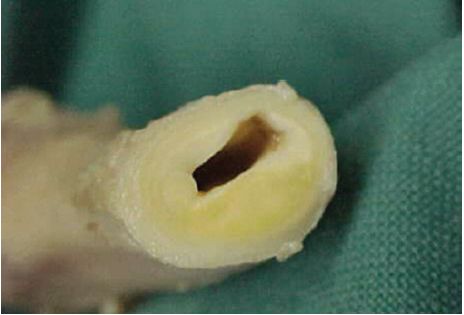
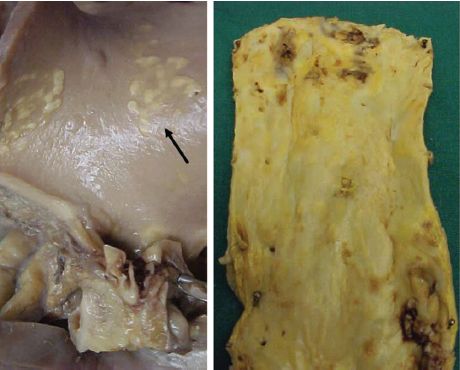
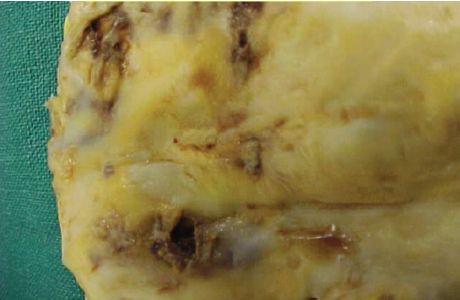
Macroscopie : lésion lenticulaire de 0,5 à 3 cm de diamètre, à surface lisse, jaunâtre, devenant à surface irrégulière et grisâtre lorsque la taille augmente (figure 4.20).
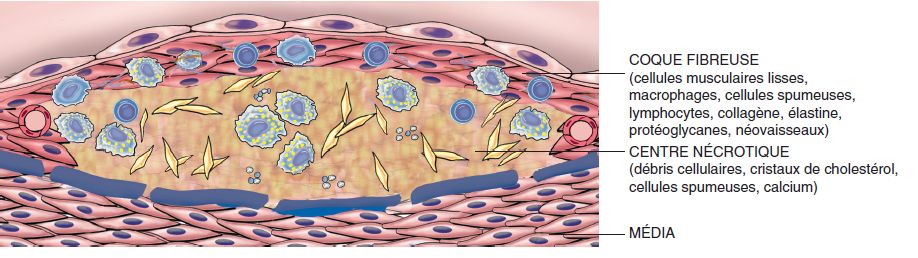
Microscopie : la lésion est formée d’un centre constitué de cellules « spumeuses » et de nécrose riche en cristaux de cholestérol situés en position extra-cellulaire (« bouillie lipidique » = athérome) et d’un territoire périphérique entourant cette zone, formé d’une fibrose (figure 4.21). Cette fibrose se densifie progressivement en séparant la nécrose centrale de l’endothélium et en dissociant la média dans les zones profondes (figure 4.22).
Les lésions d’athérosclérose constituées vont évoluer avec le temps et s’étendre progressivement : les plaques peuvent confluer et réaliser au niveau de l’aorte un aspect « d’aorte pavée ».
Au cours de son évolution, la plaque peut se calcifier, c’est-à-dire s’imprégner de sels calcaires. Les plaques peuvent se transformer en véritables « coquilles d’œuf » rendant la paroi artérielle rigide (aspects visibles sur les radiographies).
4
.
3
.
3
-
Lésions compliquées de la maladie
Ulcération de la plaque
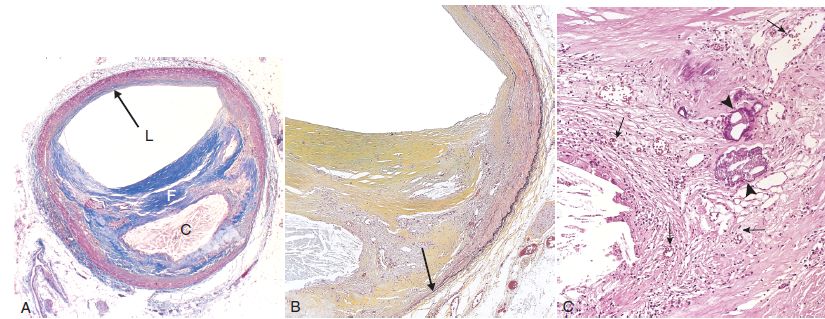
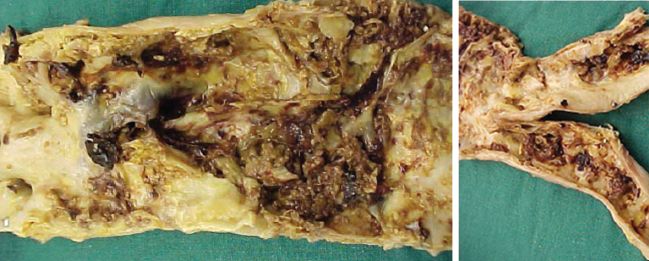
L’ulcération correspond à une destruction partielle du revêtement de la plaque (endothélium + tissu fibreux), qui met en contact le sang et le milieu interstitiel. Cette ulcération se produit soit au centre d’une plaque non calcifiée soit à la périphérie d’une plaque calcifiée (figure 4.23). Elle est plus ou moins profonde, depuis une érosion jusqu’à une ulcération creusante (rupture de plaque).
Hémorragie et hématome intraplaque
Du sang sous pression peut s’engouffrer dans la brèche créée par l’ulcération entraînant ainsi un élargissement de la brèche et la formation d’un hématome dans la plaque d’athérome. Un autre mécanisme physiopathologique est représenté par la rupture de néo-vaisseaux intraplaque, réalisant un hématome.
Thrombose sur plaque
Il existe les thromboses murales et les thromboses oblitérantes.
Un thrombus se forme au contact d’une ulcération de la plaque. Cette thrombose peut être :
- murale en raison du calibre du vaisseau et de la rapidité du courant sanguin (ex : au niveau de l’aorte thoracique) ;
- ou bien elle peut être oblitérante lorsque le calibre est plus réduit (ex : certaines thromboses coronariennes).
Toutefois, certaines thromboses oblitérantes peuvent s’observer au niveau du carrefour aortique dans les zones où le courant sanguin se ralentit et ce malgré le calibre large du vaisseau. Ces thromboses ont des répercussions sur les organes et les tissus situés en aval.
Une thrombose oblitérante est responsable de phénomènes ischémiques aigus et d’une nécrose (infarctus).
Une thrombose murale peut être responsable de phénomènes ischémiques chroniques (hypotrophie de l’organe, fibrose) ou d’un infarctus si elle est brutale et importante (figure 4.24).
Embolies et leurs conséquences
Il peut s’agir soit d’emboles de type « athéromateux » à partir d’une plaque ulcérée (réalisant parfois un syndrome des emboles cholestéroliques), soit d’emboles fibrinocruoriques à partir d’un thrombus. Ces embolies ont des conséquences ischémiques sur les tissus et organes situés en aval (peau, rein, cerveau, extrémités).
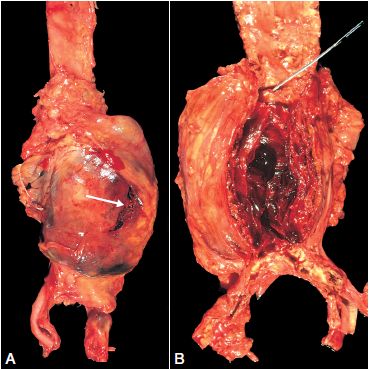
Anévrisme
Il s’agit d’une dilatation d’un vaisseau, avec une perte de parallélisme de ses parois. Cet anévrisme est dû à l’amincissement pariétal avec destruction des lames élastiques et des cellules musculaires lisses de l’artère. Les anévrismes athéromateux prédominent sur l’aorte abdominale et sont fréquemment le siège de thrombose, avec création d’embole, de fissure et risque de rupture (figure 4.25).
Corrélations anatomocliniques
Les manifestations cliniques en rapport avec la présence d’une plaque athéroscléreuse sont très inconstantes et les corrélations imprécises, ce qui rend difficile la prévision des manifestations cliniques en fonction de la taille et de l’évolution d’une plaque.
Schématiquement, les plaques non compliquées sténosantes (> ou = 70 % dans le territoire coronaire) sont associées à une symptomatologie apparaissant à l’effort (angor d’effort, claudication intermittente). Les plaques compliquées sont responsables d’une symptomatologie paroxystique et d’accidents cliniques : infarctus du myocarde, mort subite, angor de repos, accident vasculaire cérébral par exemple. Mais ces manifestations sont inconstantes et une plaque compliquée peut rester asymptomatique.
4
.
4
-
Formes anatomocliniques
4
.
4
.
1
-
Athérosclérose aortique
L’atteinte principale se situe au niveau de l’aorte sous-diaphragmatique (ou aorte abdominale). Cette atteinte peut être associée à un syndrome du carrefour aortique associant une insuffisance circulatoire des membres inférieurs (responsable d’une claudication intermittente et d’une cyanose des téguments avec abolition des pouls fémoraux) et d’une impuissance sexuelle d’installation progressive.
4
.
4
.
2
-
Athérosclérose périphérique
C’est l’athérosclérose des artères viscérales, des collatérales de l’aorte et des artères des membres inférieurs. Les conséquences sont en relation directe avec la topographie de l’atteinte artérielle :
- coronaires : angine de poitrine et infarctus du myocarde ;
- carotides et polygone de Willis : accident vasculaire cérébral ;
- artères rénales : hypertension artérielle secondaire ;
- artères des membres (membres inférieurs surtout) : claudication intermittente et gangrène sèche ;
- artères mésentériques : syndrome d’angor intestinal.
4
.
5
-
Histogenèse
L’importance majeure de l’athérosclérose en santé publique a suscité de très nombreux travaux pour tenter d’en élucider le mécanisme, et plusieurs hypothèses pathogéniques ont été élaborées.
À titre historique, on peut rappeler :
-
la théorie thrombogénique (théorie de Rokitansky)
Selon cette théorie, la lésion athéroscléreuse succéderait à l’incorporation de plaquettes dans l’intima à partir d’un microthrombus et de lipides. La dégranulation des plaquettes libère du PDGF (platelet derived growth factor) qui agit sur la multiplication des cellules musculaires lisses de la média, la lyse des plaquettes libérant également des lipides dans la paroi. L’accumulation des lipides dans la paroi résulte d’un transfert des lipoprotéines plasmatiques (essentiellement les LDL qui transportent 70 % du cholestérol plasmatique).
-
la théorie de « l’agression » (théorie de Virchow)
L’athérosclérose est la conséquence d’une lésion de l’endothélium qui provoque une infiltration plasmatique dans la paroi (« insudation »). Les exemples d’agression de l’endothélium sont multiples : hypertension artérielle, tabac (nicotine et hypoxie), agents infectieux (cytomégalovirus ; hypothèse très discutée), désordres métaboliques (anomalies du métabolisme de la méthionine et hyperhomocystinémie).
-
la théorie de la multiplication des myocytes intimaux (théorie de Ross et Barken)
Le processus athéromateux débute par une prolifération de myocytes accompagnée d’une production de tissu conjonctif et d’une accumulation de lipides. Cette prolifération se fait à partir de myocytes intimaux (présents au niveau de zones localisées appelées coussinets) ou après migration de myocytes de la média qui franchissent la limitante élastique interne. Ces myocytes se dédifférencient en myocytes de phénotype synthétique qui produisent du collagène responsable de l’apparition d’une fibrose.
En fait, l’athérosclérose est une maladie complexe mettant en jeu de multiples facteurs exogènes et endogènes interférant entre eux et aboutissant à une lésion commune d’infiltration lipidoprotidoglucidique et macrophagique de la paroi artérielle, avec sclérose. Les hypothèses pathogéniques contemporaines incorporent des éléments des trois théories précédentes, qui se complètent mutuellement et participent à des degrés variables à la constitution des lésions, en fonction des facteurs de risque en présence.
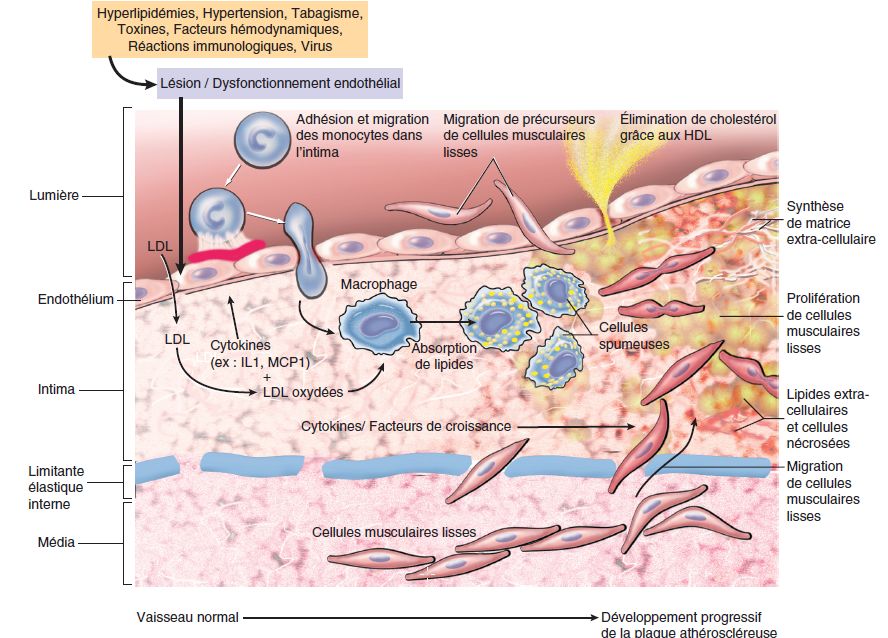
On considère actuellement que l’athérosclérose est une réponse inflammatoire chronique de la paroi artérielle à une agression endothéliale initiale dont la progression serait entretenue par des interactions entre les lipoprotéines plasmatiques, les monocytes-macrophages, les lymphocytes T et les constituants de la paroi artérielle (figure 4.26). En effet, des cellules inflammatoires sont présentes au sein des lésions, ce qui souligne le rôle du processus inflammatoire dans le développement lésionnel. De plus, des phénomènes inflammatoires sont également mis en cause dans la survenue des complications.
4
.
6
-
Conclusion
Cette maladie des grosses et moyennes artères est extrêmement fréquente et constitue, notamment en France, un problème de santé publique. L’évolution progressive et irréversible des lésions anatomopathologiques de l’athérosclérose conduit inexorablement à des complications cliniques graves. Les facteurs de risque sont multiples et l’histogénèse complexe fait intervenir de nombreux facteurs exogènes et endogènes.
4
.
7
-
Autres lésions histologiques artérielles
-
La hyalinose : il s’agit d’un épaississement intimal caractérisé en microscopie optique par un aspect homogène, vitreux et éosinophile. Elle est assez fréquente chez les sujets âgés et est plus étendue et plus sévère chez les sujets hypertendus. Elle est également fréquente chez les patients diabétiques chez qui elle est un élément de la microangiopathie diabétique.
-
La nécrose fibrinoïde : il s’agit d’un aspect éosinophile et homogène de la paroi, ± avec disparition des cellules musculaires lisses (elle est rencontrée dans certaines maladies artérielles de nature inflammatoire comme la périartérite noueuse et la maladie de Wegener – voir plus loin).
-
L’artériosclérose : il s’agit d’un épaississement intimal diffus sans dépôt lipidique entrant dans le cadre des modifications liées au vieillissement, à l’hypertension artérielle. Son extension est plus diffuse que celle de l’athérosclérose. Il ne faut donc pas confondre artériosclérose et athérosclérose.
-
La médiacalcose (surcharge calcique de la média, surtout chez les sujets diabétiques, insuffisants rénaux ou hypercalcémiques). Cette médiacalcose (ou maladie de Mönckeberg) se caractérise par l’apparition de calcifications débutant sur la limitante élastique interne puis s’étendant à toute la média.


5/7