2
-
Tumeurs conjonctives
La classification des tumeurs conjonctives repose actuellement sur le type de tissu formé par la tumeur (différenciation) et non plus sur la cellule à partir de laquelle la tumeur est supposée naître (histogénèse). Chaque type tumoral est divisé en tumeurs bénignes et malignes, et pour certains types apparaît une troisième catégorie : les tumeurs de malignité intermédiaire.
Les tumeurs bénignes conjonctives sont beaucoup plus fréquentes (de l’ordre de 100 : 1) que les tumeurs malignes conjonctives. Elles sont habituellement de petite taille, superficielles. Elles ne métastasent pas, mais peuvent récidiver localement si l’exérèse est incomplète. Classiquement, il n’y a pas de nécrose tumorale, ni d’atypie cyto-nucléaire et les mitoses sont rares.
Les tumeurs malignes conjonctives sont appelées sarcomes. Elles sont très rares (environ 1 % des cancers). Si les cellules tumorales sont peu différenciées, il est parfois difficile d’en préciser la nature (utilité de l’immunohistochimie, de la biologie moléculaire, voire de la microscopie électronique). L’évolution peut être rapide avec extension locale et métastases précoces par voie hématogène.
Il peut être difficile d’affirmer la bénignité ou la malignité d’une tumeur conjonctive bien différenciée.
Le rôle du pathologiste est :
- d’établir un diagnostic ;
- d’analyser les éléments du pronostic ;
- d’évaluer la qualité de l’exérèse (examen des limites) et/ou la réponse à une chimiothérapie.
Ceci nécessite une étroite collaboration avec les cliniciens pour connaître les renseignements cliniques (âge, localisation et taille tumorales…), les données de l’imagerie, les modalités évolutives, les antécédents et les éventuels traitements réalisés.
Lors de l’exérèse, le chirurgien doit orienter la pièce et la transmettre sans fixateur au pathologiste pour qu’un prélèvement puisse éventuellement être analysé en cytogénétique ou congelé.
L’examen macroscopique est fondamental. Il doit être soigneux avec repérage des limites d’exérèse à l’encre de chine et échantillonnage suffisant pour analyser les différents aspects de la tumeur.
L’analyse histologique appréciera :
- la morphologie des cellules tumorales (fusiformes, rondes) ;
- l’existence d’une différenciation ;
- l’importance et l’aspect de la vascularisation et du stroma ;
- la présence de remaniements (nécrose, calcification, hémorragie…).
Les facteurs pronostiques importants sont :
- le type histologique ;
- la taille de la tumeur ;
- la localisation (superficielle ou profonde) de la tumeur ;
- l’état des limites de la résection chirurgicale ;
- le grade histopronostique.
Le grade histopronostique des sarcomes des tissus mous comporte trois grades de malignité et repose sur l’évaluation de trois paramètres :
- le degré de différenciation tumorale ;
- l’activité mitotique ;
- la proportion de tissu tumoral nécrosé.
Les sarcomes de grade 1 correspondent aux tumeurs très différenciées de potentiel métastatique faible, les sarcomes de grade 3 aux tumeurs peu différenciées de potentiel métastatique élevé.
 Grade histopronostique des sarcomes .
Grade histopronostique des sarcomes .
La classification des tumeurs conjonctives a été considérablement modifiée ces 15 dernières années par l’apport des techniques immunohistochimiques et cytogénétiques. L’identification d’une tumeur conjonctive repose sur l’association de plusieurs critères : présentation anatomoclinique particulière, aspects morphologiques, immunohistochimiques et/ou ultrastructuraux caractéristiques et anomalies chromosomiques particulières.
2
.
1
-
Tumeurs des tissus fibreux (fibroblastiques ou myofibroblastiques)
Ces tumeurs ont en commun une prolifération de fibroblastes (vimentine positifs) qui peuvent prendre une différenciation fibrohistiocytaire (CD68 positifs), ou myofibroblastique (actine positive).
2
.
1
.
1
-
Fibromes
Ce sont des proliférations bénignes, d’évolution lente. Ils sont constitués de fibroblastes associés à une plus ou moins grande quantité de fibres collagènes disposées en faisceaux. Ils peuvent siéger n’importe où dans le tissu conjonctif commun, mais s’observent surtout dans la peau et les voies aériennes supérieures (fosses nasales, rhinopharynx) où ils sont souvent très vascularisés.
Le fibrome mou ou molluscum pendulum est une petite tumeur cutanée très fréquente, de consistance molle et allongée, parfois pédiculée, souvent située sur le cou, le thorax ou les aisselles.
2
.
1
.
2
-
Fibromatoses
Ce sont des proliférations fibroblastiques multifocales, évolutives, développées à partir des aponévroses, envahissant et détruisant les muscles, pouvant être volumineuses.
La maladie de Dupuytren est une fibromatose nodulaire rétractile de l’aponévrose palmaire. Elle est souvent bilatérale. L’atteinte peut aussi être plantaire ou génitale (pénis).
La tumeur desmoïde (desmos = tendon) (ou fibromatose desmoïde) correspond à une prolifération fibroblastique et myofibroblastique peu dense associée à du tissu collagène hyalinisé abondant. De siège intra ou extra-abdominal, elle est souvent très mal limitée et envahit les tissus avoisinants. Son exérèse doit si possible être large pour éviter les fréquentes récidives locales, mais elle est souvent difficile à réaliser ou au prix d’une chirurgie mutilante.
2
.
1
.
3
-
Tumeur fibreuse solitaire
Cette tumeur a été initialement décrite dans la plèvre puis en situation sous-cutanée au niveau de la tête et du tronc, dans les méninges, etc.
C’est une tumeur bénigne, à cellules fusiformes, richement vascularisée. Les cellules tumorales expriment le CD34, le CD99 et BCL2.
2
.
1
.
4
-
Dermatofibrosarcome de Darier et Ferrand
Il est actuellement classé parmi les tumeurs fibrohistiocytaires. C’est une tumeur cutanée rare, nodulaire, mal limitée. Les cellules tumorales sont positives avec le CD34.
2
.
1
.
5
-
Fibrosarcome
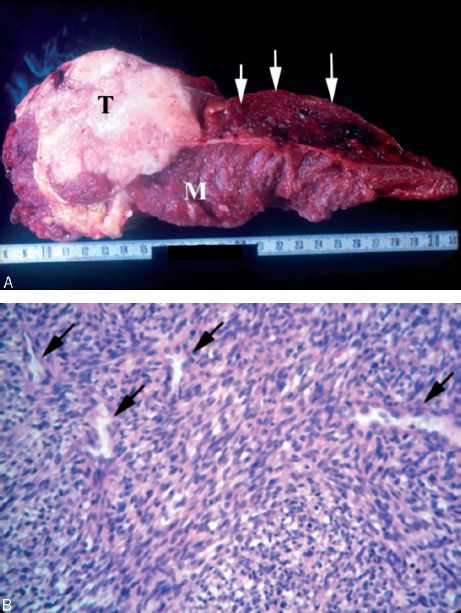
C’est une prolifération conjonctive maligne à différenciation purement fibroblastique qui se développe dans les membres ou le tronc. L’évolution se fait vers la récidive locale et les métastases à distance (figure 11.8).
Dans les formes bien différenciées la frontière avec un fibrome envahissant est imprécise. Le diagnostic différentiel avec des lésions inflammatoires, réactionnelles, non tumorales (fasciites) peut être difficile.
2
.
2
-
Tumeurs adipeuses
Ce sont des tumeurs fréquentes.
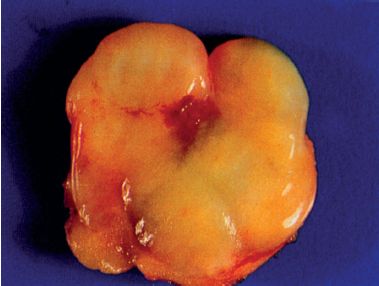
Les lipomes sont des tumeurs bénignes, superficielles, qui s’observent surtout après 45 ans. Ils sont constitués d’adipocytes, ressemblant à du tissu adipeux mature. L’aspect macroscopique est celui d’une tumeur homogène, flasque, jaunâtre (figure 11.9).
Les liposarcomes sont des tumeurs fréquentes des tissus mous. Ils peuvent être de trois types : bien différencié, myxoïde et pléomorphe. Les liposarcomes bien différenciés sont des masses à croissance lente, souvent bien limitées, parfois plurinodulaires. Selon la topographie de la tumeur, il peut être difficile, voire impossible, d’en réaliser une exérèse complète (rétropéritoine). Les récidives locales sont donc fréquentes, itératives. Les liposarcomes bien différenciés peuvent également subir un phénomène de « dédifférenciation », qui correspond à l’apparition d’un contingent sarcomateux agressif au sein de la tumeur.
Le liposarcome myxoïde se développe dans les tissus mous des membres, mais pas dans le rétropéritoine. Il peut être de bas ou de haut grade de malignité. Il est caractérisé par une anomalie génétique spécifique, la translocation t(12 ; 16) (q13 ; p11).
Enfin, le liposarcome pléiomorphe est une tumeur peu différenciée, de haut grade de malignité, d’emblée agressive et associée à un risque métastatique élevé.
2
.
3
-
Tumeurs musculaires
On distingue les tumeurs conjonctives développées aux dépens des muscles lisses (léiomyomes, léiomyosarcomes) de celles développées à partir des muscles striés (rhabdomyomes, rhabdomyosarcomes).
Tumeurs musculaires lisses
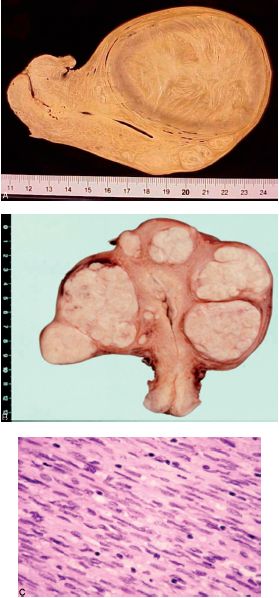
Les léiomyomes sont des tumeurs musculaires lisses bénignes, fréquentes, bien différenciées. Ils sont extrêmement fréquents dans le corps utérin : les léiomyomes utérins, souvent multiples, parfois appelés à tort fibromes, sont très fréquemment observés chez la femme en période péri- ou post-ménopausique et nécessitent parfois de réaliser une hystérectomie (à cause de leur taille, leur nombre, leur nécrobiose ou en raison de métrorragies) (figures 11.10A,B,C). Ils peuvent aussi être localisés dans le tube digestif ou les parois vasculaires.
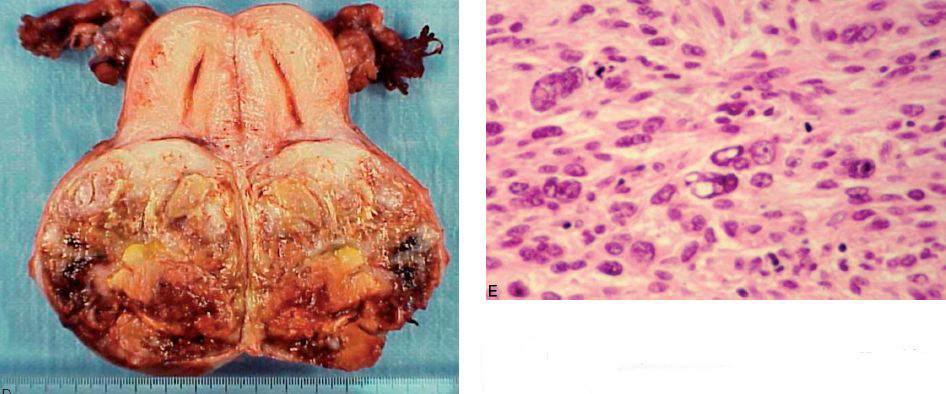
Les léiomyosarcomes sont des tumeurs musculaires lisses malignes. Elles surviennent électivement chez l’adulte, tant au niveau de la peau que des viscères creux, dont l’utérus (figures 11.10D et E).
Tumeurs musculaires striées
Les rhabdomyomes sont des tumeurs bénignes rares (figure 11.11). Les rhabdomyomes cardiaques sont souvent associés à la sclérose tubéreuse de Bourneville.
Les rhabdomyosarcomes sont des tumeurs malignes plus ou moins bien différenciées. Les rhabdomyosarcomes sont plus fréquents chez l’enfant que chez l’adulte et ont souvent un mauvais pronostic, nécessitant une exérèse précoce et large. Ils se développent préférentiellement au niveau des cavités céphaliques (orbite, nez, sinus, oreille) ou de la sphère urogénitale (vessie, prostate, vagin, cordon spermatique). Plus rarement, ils sont intramusculaires au niveau des muscles proximaux des membres.
2
.
4
-
Tumeurs vasculaires
Angiomes
Il s’agit de tumeurs vasculaires bénignes, caractérisées par une prolifération de vaisseaux néoformés entourés de tissu conjonctif. On en distingue deux types, les hémangiomes et les lymphangiomes.
Hémangiomes
Ils sont faits de vaisseaux sanguins et comprennent selon le type histologique de ces vaisseaux :
- les hémangiomes capillaires (sont également considérés comme des dysplasies tissulaires lors du développement ou des hamartomes). Ils sont composés de la juxtaposition de nombreux capillaires ayant ou non une lumière centrale où se trouvent des hématies. Ils siègent principalement sur la peau et les muqueuses ;
- les hémangiomes caverneux qui forment de larges cavités kystiques juxtaposées remplies de sang, séparées par des lames collagènes plus ou moins épaisses et bordées par des cellules endothéliales. Ils siègent dans la peau, le foie, les muscles (langue).
Lymphangiomes
Il s’agit toujours de tumeurs bénignes de l’enfant constituées de vaisseaux lymphatiques qui forment des cavités de taille très variée, remplies de lymphe, auxquelles s’associent souvent des ébauches imparfaites de ganglion lymphatique et des troncs veineux anormaux. Leur siège d’élection est cervico-médiastinal unilatéral, plus rarement mésentérique.
Angiomatoses
La présence d’hémangiomes multiples caractérise divers syndromes.
 Angiomatoses.
Angiomatoses.
2
.
5
-
Angiosarcomes
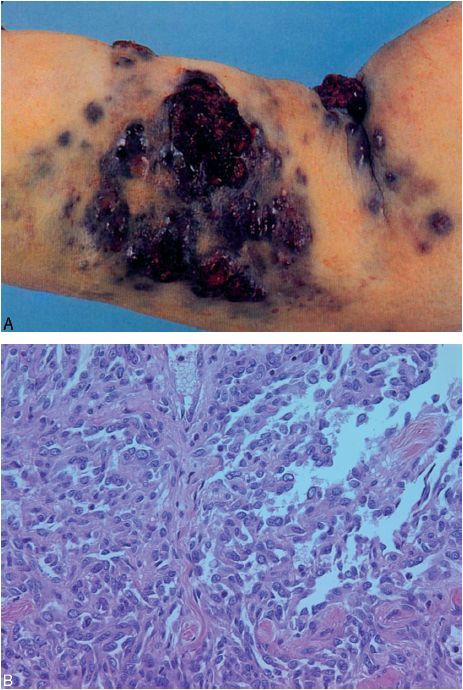
Ce sont des tumeurs malignes souvent peu différenciées qui prédominent sur la peau et dans les tissus mous (figure 11.12), parfois les viscères (foie). Un angiosarcome peut parfois se développer sur un lymphœdème chronique du bras, chez les patientes opérées d’un cancer du sein : c’est le syndrome de Stewart-Treves.
On en rapproche le sarcome de Kaposi qui réalise une prolifération de cellules fusiformes, creusée de fentes vasculaires séparées par du tissu collagène, parsemée de macrophages surchargés en hémosidérine. Cette tumeur est habituellement unique et localisée dans le derme chez les sujets âgés. Une forme d’évolution rapide avec localisations multiples (cutanées mais aussi viscérales) est décrite en Afrique mais aussi chez les sujets atteints de SIDA. Une origine infectieuse est démontrée. L’agent étiologique est un virus du groupe herpès (HHV-8 ou Human herpès virus 8).
2
.
6
-
Tumeurs de différenciation incertaine
La différenciation et l’histogenèse de plusieurs groupes de tumeurs conjonctives restent incertaines, voire inconnues. Parmi ces tumeurs, on trouve le synovialosarcome, qui, contrairement à ce qui avait été suggéré initialement, ne se développe pas aux dépens d’un revêtement synovial. Le synovialosarcome est avant tout une tumeur des tissus mous profonds des membres mais peut aussi toucher certains organes comme le poumon et le rein. Histologiquement, il se caractérise par une prolifération souvent biphasique, associant une composante conjonctive et une composante épithéliale. Il est caractérisé par une translocation spécifique t(X ; 18), dont la mise en évidence constitue un outil diagnostique important.
2
.
7
-
Tumeurs du squelette
Tumeurs ostéoformatrices
-
Tumeurs ostéoformatrices bénignes : ostéome ostéoïde et ostéoblastome
L’ostéoblastome partage avec l’ostéome ostéoïde un même aspect histopathologique, associant des ostéoblastes sans atypie, une ostéogenèse immature et un stroma richement vascularisé. Ces deux entités diffèrent par contre par leurs présentations radio-cliniques. L’ostéome ostéoïde est une lésion de petite taille, peu évolutive, caractérisée par une symptomatologie douloureuse, alors que l’ostéoblastome constitue un véritable processus tumoral expansif, parfois volumineux et pouvant être pris à tort pour une tumeur maligne.
-
Tumeurs ostéoformatrices malignes : les ostéosarcomes
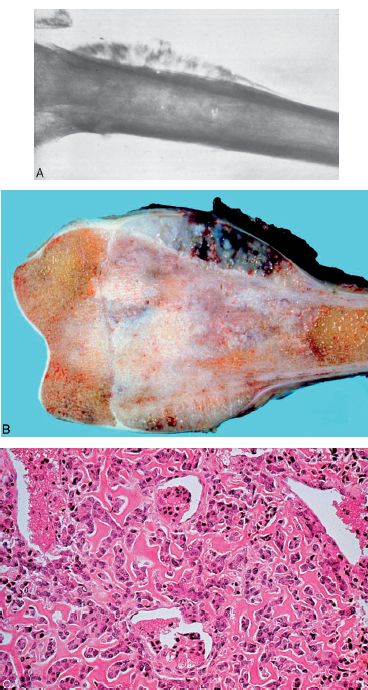
Ce sont des tumeurs malignes fréquentes de l’adolescence, lors de la croissance des membres (métaphyse des os longs). La prolifération tumorale est constituée d’ostéoblastes atypiques, produisant un os immature. À l’opposé des tumeurs ostéoformatrices bénignes, l’ostéosarcome détruit le tissu osseux préexistant et infiltre les parties molles (figure 11.13).
Leur évolution est rapide et les métastases pulmonaires fréquentes. Chez le sujet jeune, les garçons sont électivement touchés, notamment au niveau des membres inférieurs, près du genou (extrémité inférieure du fémur et supérieure du tibia). Chez le sujet âgé, ces tumeurs surviennent fréquemment sur une lésion préexistante (maladie de Paget).
Tumeurs cartilagineuses
-
Tumeurs cartilagineuses bénignes : ostéochondrome et chondrome
L’ostéochondrome (ou exostose ostéogénique) est la plus fréquente des lésions osseuses. Elle a une architecture caractéristique associant de dehors en dedans, une coiffe cartilagineuse, dont l’aspect histologique est proche de celui d’un cartilage de croissance et un tissu osseux d’architecture trabéculaire constituant le corps de l’exostose.
Le chondrome est constitué de plusieurs nodules cartilagineux, en général de petite taille, renfermant des chondrocytes sans atypie. Le chondrome respecte l’os pré-existant.
La maladie des exostoses multiples et les chondromatoses multiples ont un risque de dégénérescence maligne qui justifie la mise en place d’une surveillance et l’exérèse de toute lésion se modifiant, par définition suspecte.
-
Tumeurs cartilagineuses malignes : les chondrosarcomes
Ce sont des tumeurs rares de l’adulte, souvent âgé, d’évolution lente, qui atteignent les os plats des ceintures. Ils sont constitués de nodules cartilagineux de taille importante, renfermant des chondrocytes atypiques. À l’opposé des tumeurs cartilagineuses bénignes, le chondrosarcome détruit le tissu osseux préexistant et infiltre les parties molles. Les chondrosarcomes de bas grade ont une malignité locale alors que les chondrosarcomes de grade intermédiaire et de haut grade présentent un risque dissémination métastatique pulmonaire.
Ce sont des tumeurs rares, dérivées de reliquats de la notochorde. Elles surviennent électivement au niveau du rachis, en particulier au niveau du sacrum et de la région sphéno-occipitale. Ce sont des tumeurs malignes, de croissance lente et d’évolution surtout locale, dont l’exérèse complète est souvent difficile et le pronostic défavorable en raison de l’extension locale.
Le sarcome d’Ewing est une tumeur maligne osseuse intramédullaire, lytique, infiltrant la corticale avec souvent une importante réaction périostée, qui peut toucher tous les os y compris les petits os, les os plats et les vertèbres. La prolifération tumorale est d’aspect peu différencié, « à petites cellules rondes et bleues ». Les cellules contiennent souvent du glycogène (coloré par le PAS) et expriment l’antigène de groupe sanguin Mic-2. Il existe de façon quasi constante une translocation t(11 ; 22). La mise en évidence par biologie moléculaire du gène de fusion est une aide importante au diagnostic.
Le terme de « tumeur neuroectodermique périphérique (PNET pour Peripheral neuroectodermal tumor) » recouvre le sarcome d’Ewing ainsi que des tumeurs identiques de siège extra-osseux, plus rares.
Ces différentes entités, de siège osseux ou extra-osseux, sont aujourd’hui regroupées sous l’appellation « tumeurs de la famille Ewing ».
2
.
8
-
Tumeurs mésothéliales
Les tumeurs bénignes pleurales (fibromes mésothéliaux de la plèvre viscérale) sont rares.
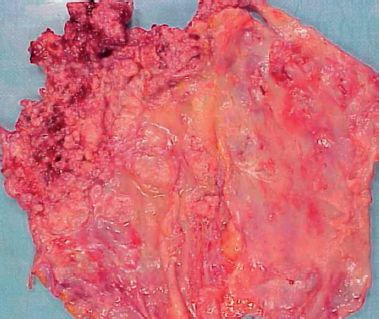
Les mésothéliomes malins sont surtout pleuraux (plus rarement péritonéaux ou péricardiques) et sont dans leur immense majorité liés à une exposition à l’amiante (asbestose) dans les 20 ans précédents. Ils donnent au début une prolifération mésothéliale papillaire pariétale, puis ultérieurement une atteinte massive de tous les feuillets de la plèvre avec formation de nodules et masses multiples (figure 11.14). Actuellement, l’évolution est le plus souvent rapidement fatale.
Microscopiquement, il existe une prolifération souvent biphasique faite de cellules fusiformes et de fentes épithéliales. L’immunohistochimie est souvent indispensable pour affirmer le diagnostic et exclure la possibilité d’une métastase pleurale (diagnostic différentiel).
2
.
9
-
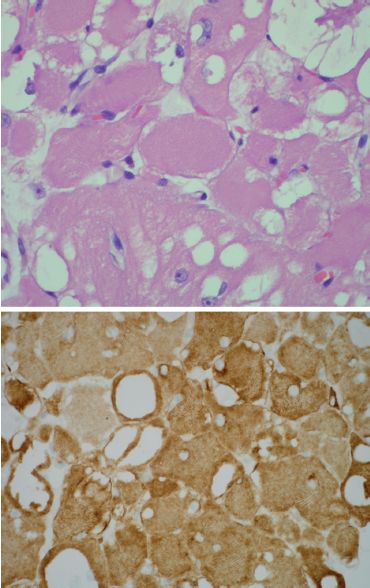
Tumeurs stromales digestives
Ces tumeurs se développent principalement au niveau de l’estomac et de l’intestin grêle et sont parfois dénommées en utilisant l’acronyme anglo-saxon « GIST : Gastro-intestinal stromal tumor » (figure 11.15). Elles dérivent des cellules interstitielles de Cajal, qui sont responsables du péristaltisme du tube digestif. Les tumeurs stromales digestives sont fortement associées à une expression et une activation de l’oncogène KIT, ou plus rarement du PDGFRα.
Le pronostic est variable et reste souvent incertain après l’analyse histopathologique. On doit généralement les considérer comme des tumeurs potentiellement malignes. Toutefois, les tumeurs de petites tailles avec peu de mitoses ont le plus souvent un comportement bénin (guérison définitive après l’exérèse), alors que les tumeurs volumineuses et riches en mitoses peuvent donner des métastases et conduire au décès.
2/5






 Grade histopronostique des sarcomes
Grade histopronostique des sarcomes