4 - Hyperthyroïdies et traitements par hormones thyroïdiennes
L’hyperthyroïdie constitue une cause classique d’ostéoporose secondaire. De nos jours, la précocité du diagnostic et l’efficacité des traitements font que la phase d’hyperthyroïdie est souvent transitoire et les signes osseux exceptionnellement révélateurs, ou au premier plan. L’hyperthyroïdie reste une des causes fréquentes d’ostéoporose secondaire, surtout chez le sujet âgé ou la femme ménopausée. Elle est souvent paucisymptomatique, ce qui justifie le dosage systématique de la TSH dans la recherche étiologique d’une ostéoporose secondaire.
Les traitements par les hormones thyroïdiennes (HT) font partie des traitements hormonaux les plus communément administrés chez la femme. Le risque osseux de ces traitements paraît cependant faible.
A. Physiopathologie de l’atteinte osseuse
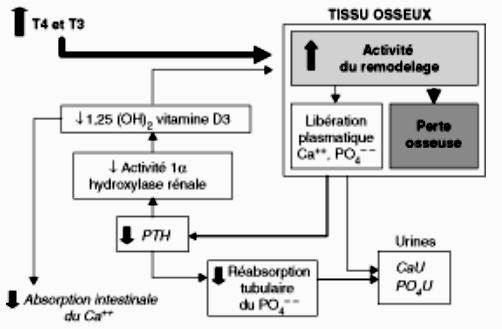
Les hormones thyroïdiennes augmentent le remodelage osseux (figure 8.3). Cet effet résulte d’une augmentation du recrutement des unités élémentaires de remodelage (bone multicellular unit ou BMU) et de leur fréquence d’activation. Il existe une balance négative entre résorption et formation osseuse qui prédomine sur l’os cortical, où l’on note une augmentation du diamètre des canaux de résorption, conduisant à une accentuation de la porosité corticale et à une réduction de l’épaisseur corticale. Au niveau de l’os trabéculaire, cette hyperrésorption osseuse entraîne une diminution de l’épaisseur trabéculaire et une augmentation du risque de perforations trabéculaires.
Effets sur le tissu osseux et le métabolisme phosphocalcique (Ca++).
CaU : calciurie ; PO4U : phosphaturie.
Au plan cellulaire, l’effet osseux des HT peut découler d’une action directe sur les ostéoclastes ou d’une augmentation de la production ostéoblastique de différents facteurs de croissance et/ou cytokines, qui réguleront en retour la fonction ostéoclastique. Les mécanismes de la prépondérance corticale de l’atteinte osseuse de l’hyperthyroïdie sont encore mal expliqués. Elle pourrait être liée à l’augmentation, plus importante dans l’os cortical (fémur) que trabéculaire, de certains marqueurs géniques des ostéoclastes (phosphatase acide tartrate-résistante) et des ostéoblastes (ostéocalcine, ostéopontine, phosphatase alcaline). Des travaux récents suggèrent de plus que la TSH pourrait agir comme un élément de régulation négative du remodelage osseux.
B. Masse osseuse et risque fracturaire
Une diminution de la DMO de 10 à 20 %, par rapport à des sujets de même âge et de même sexe, a été rapportée dans beaucoup d’études chez les sujets hyperthyroïdiens. Cependant, la prévalence des fractures attribuables à l’hyperthyroïdie reste mal appréciée. Certaines études notent que les femmes ayant des antécédents d’hyperthyroïdie auraient tendance à présenter des fractures ostéoporotiques à un âge plus jeune, d’autres que le risque relatif de fracture de l’extrémité supérieure du fémur serait pratiquement doublé. En fait, ces études ont intéressé des patientes à une époque où le diagnostic et le traitement étaient plus tardifs qu’aujourd’hui, et il est vraisemblable qu’actuellement très peu d’hyperthyroïdies évoluent assez longtemps pour entraîner une atteinte osseuse significative. Le traitement médical, ou chirurgical, de l’hyperthyroïdie s’associe à une correction rapide de l’hyper-remodelage osseux et à une récupération progressive du contenu minéral osseux.
L’administration de doses élevées d’HT, telle qu’est est réalisée dans le traitement du cancer thyroïdien différencié hormonodépendant, est susceptible d’augmenter le risque d’ostéoporose. Cependant, les dosages ultrasensibles de la TSH permettent de déterminer, avec plus de facilité qu’au préalable, la dose minimale d’HT permettant de mettre au repos l’axe thyréotrope tout en n’induisant pas trop d’hyperthyroïdie infraclinique. Les études les plus récentes utilisant des méthodes de mesure plus fiables, telle la DEXA, n’ont pas authentifié de diminution significative de la densité osseuse vertébrale chez les patients recevant un traitement à visée suppressive ; cependant, une atteinte fémorale modérée avec une diminution de 5 à 10 % de la densité osseuse a été parfois rapportée. La signification clinique d’une telle diminution, en termes de risque fracturaire, apparaît cependant négligeable, tout au moins chez les sujets ne présentant pas de facteurs de risque additionnels. La posologie des HT doit être adaptée au pronostic du cancer thyroïdien de manière à limiter le retentissement osseux chez les patients en rémission et à faible risque de récidive, chez qui la TSH peut être ramené dans la moitié inférieure de la normale.
Par ailleurs, aucune étude ne documente une augmentation de l’incidence fracturaire chez les patients hypothyroïdiens traités par hormones thyroïdiennes.
C. Prévention et traitement
Même si la correction rapide de l’hyperthyroïdie limite dans la plupart des cas (notamment chez le sujet jeune) l’impact osseux des HT, la réalisation d’un examen densitométrique permettant de documenter cette atteinte osseuse doit être préconisée. La mise en route d’un traitement de prévention de la perte osseuse n’apparaît pas nécessaire dans la majorité des cas, sauf chez les sujets âgés chez lesquels la mise en route d’un traitement de prévention, notamment par un bisphosphonate (alendronate, risédronate), doit être alors plus particulièrement recommandée.
La surveillance densitométrique des patients recevant un traitement suppressif de la fonction thyroïdienne est également justifiée, d’autant qu’il s’agit de traitements définitifs et/ou s’adressant à des femmes ménopausées, ou à des patients âgés déjà déminéralisés. La mise en route d’un traitement de prévention doit là également être envisagée chez les patients les plus à risque de fracture de l’extrémité supérieure du fémur. La présence d’une élévation importante des bio-marqueurs osseux, témoignant d’un haut niveau de remodelage, peut aider à la décision thérapeutique.