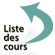- Pré-requis et Objectifs
- Cours
- Annexes
- Votre Avis
- Ressources Enseignants
4 - Examens complémentaires orientés en fonction du contexte
4 . 1 - Exploration du cycle ovulatoire
1. Exploration hormonale (++)
L’exploration est différente selon le contexte.
En cas d’aménorrhée ou d’irrégularités menstruelles, on cherche d’abord à préciser leur mécanisme (cf. chapitre 19 : « Aménorrhée »). Le test à la progestérone permet d’apprécier le degré de carence estrogénique : pas de carence si le test est positif, sinon carence sévère (quelle que soit la cause de l’aménorrhée). Les dosages les plus utiles dans un premier temps sont ceux de l’estradiol (E2), de LH (hormone lutéinisante), de FSH et de prolactine (PRL) plasmatiques.
Si les cycles sont réguliers, on cherche à préciser leur caractère ovulatoire par un dosage de progestérone plasmatique, 6 à 7 jours après le décalage de la courbe thermique ou à J22-J23 du cycle (++).
2. Échographie ovarienne (+++)
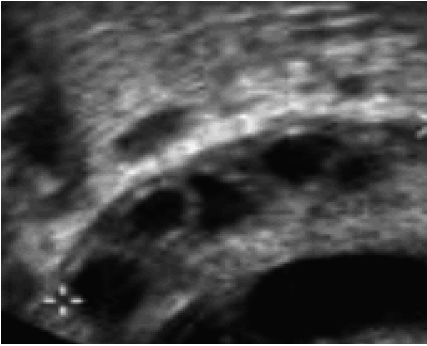
Par voie endovaginale, elle précise la taille et l’aspect des ovaires et permet d’évaluer le compte des follicules antraux (facteur pronostique < 5, mauvais ; entre 5 et 10, bon ; > 10/ovaire, syndrome des ovaires polymicrokystiques avec un aspect en couronne et une hypertrophie du stroma ovarien) (figure 4.3). Elle permet aussi de mesurer l’épaisseur de la muqueuse utérine et de montrer la présence d’éventuel(s).
Fig. 4.3. Échographie endovaginale
Fig. 4.3. Échographie endovaginale
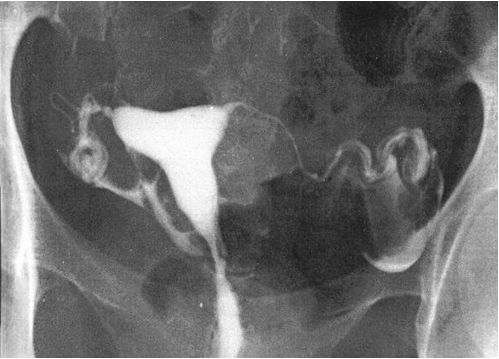
4 . 2 - Hystérographie (+++)
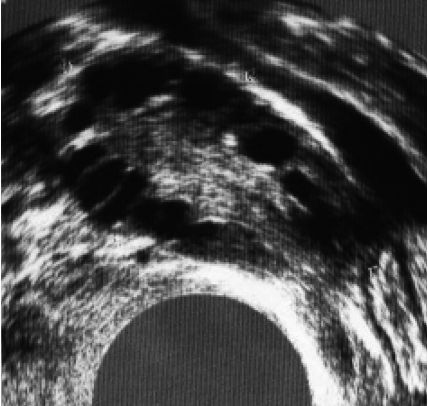
L’hystérographie (HSG) précise l’intégrité et la perméabilité de l’utérus et des trompes. Elle doit être obligatoirement effectuée en dehors de toute infection génitale évolutive (risque d’endométrite ou de salpingite) et après avoir écarté une grossesse. Elle est réalisée en phase folliculaire moyenne vers le 8e-10e jour du cycle. Elle permet d’apprécier la cavité utérine, l’état et la perméabilité des trompes ainsi que le passage plus ou moins facile du produit de contraste dans la cavité péritonéale (figure 4.4).
Fig. 4.4. Hystérographie
4 . 3 - Spermogramme (+++) et spermocytogramme
C’est l’examen fondamental chez l’homme. Les trois paramètres essentiels sont : la concentration, la mobilité et la morphologie des spermatozoïdes. Les principales caractéristiques du sperme normal ainsi que les principales anomalies retrouvées chez les hommes infertiles sont indiquées dans le tableau 4.I.
Le spermogramme tient la première place dans le bilan d’une infertilité masculine. Mais cet examen doit être interprété de façon critique. En effet, l’extrême variabilité des paramètres, à la fois inter et intra-individuelle, rend difficile l’établissement de critères précis de normalité. Les conditions de recueil doivent être soigneusement contrôlées. Le sperme doit être émis au laboratoire, par masturbation, après trois jours d’abstinence. Les critères de l’OMS (cf. tableau 4.I) sont donnés à titre indicatif.
On parle d’oligospermie lorsque la numération est inférieure à 20 millions/mL. Mais plusieurs études prospectives indiquent que la fécondité ne chute significativement qu’en dessous de 5 millions/mL. De plus, il a été montré que la fécondance est davantage corrélée à la mobilité et au pourcentage des atypies cellulaires. Il faut savoir rechercher des agglutinats et noter l’existence d’une leucospermie d’un volume séminal < 2 mL.
Une affection même bénigne et de courte durée, tel un épisode grippal, est susceptible de retentir sur les caractéristiques du sperme émis 2 à 3 mois plus tard, en raison de la durée de 74 jours du cycle de la spermatogenèse. Enfin, il est parfaitement établi que, même dans des conditions strictement physiologiques, les caractéristiques du sperme sont soumises à d’importantes fluctuations. Lorsqu’il apparaît pathologique, le spermogramme doit être recontrôlé 3 mois plus tard.
Des marqueurs des glandes annexes peuvent être mesurés dans le liquide séminal :
- phosphatases acides (prostate) ;
- carnitine (épididyme) ;
- fructose (vésicules séminales) ;
- modification du taux de ces marqueurs, signant l’atteinte probable des glandes correspondantes.
Tableau 4.I.Paramètres du spermogramme (selon l’OMS)
| Paramètres | Sperme normal | Sperme anormal |
| Mobilité | > 50 % | < 50 % (asthénozoospermie) |
| Morphologie | > 30 %* | < 30 % (tératozoospermie) |
| Numération | > 20 '106/mL | < 20 '106/mL (oligospermie) 0 (azoospermie) |
| Volume éjaculat | > 2 mL | < 2 mL (hypospermie) |
| * en% de formes normales. | ||
Ces mesures permettent de préciser le niveau de l’obstacle sur les voies excrétrices.
4 . 4 - Exploration hormonale
Chez l’homme, l’exploration hormonale simple permet de diagnostiquer un déficit gonadotrope, ou une insuffisance testiculaire primitive par les dosages de testostérone, de LH, de FSH et si possible d’inhibine B et de SHBG (sex hormone-binding globulin) plasmatiques. La PRL doit être mesurée en cas de dysfonction sexuelle ou de gynécomastie non expliquée.
4 . 5 - Test post-coïtal (test de Hühner)
Il est réalisé près de 2 heures après un rapport sexuel. Il explore l’interaction entre mucus cervical et spermatozoïdes, déposés lors du rapport, dans la glaire de qualité optimale en préovulatoire. Il doit être fait pour dépister une pathologie de la glaire cervicale, préciser les caractéristiques de mobilité de spermatozoïdes in vivo et rechercher une incompatibilité immunologique entre le sperme et le mucus. Il est réalisé après une abstinence de 3 à 4 jours, puis est lu en phase préovulatoire, 4 à 8 heures après un rapport sexuel. Il est en général réalisé lorsque l’évaluation initiale n’a pas montré d’anomalie évidente.
1. Réalisation du test
Ce test nécessite :
- la surveillance de la courbe, associée à une échographie ovarienne de maturation folliculaire préovulatoire (taille du follicule dominant de 18 à 20 mm, endomètre d’épaisseur de 7 à 10 mm) ;
- une glaire abondante et filante ;
- un dosage d’estradiol plasmatique entre 150 et 300 ng/L.
Il comporte l’examen de la glaire cervicale, appréciée avec une pince dont on étend les branches pour coter la filance (> 10 cm en situation normale et en période d’ovulation), l’abondance, la transparence et la cristallisation en feuille de fougère au microscope ainsi que l’évaluation de la mobilité des spermatozoïdes : progressive, mobilité sur place, ou immobilité.
2. Résultats
Pour avoir des résultats normaux, 5 à 10 spermatozoïdes à mobilité progressive par champ doivent être observés au grossissement 400.
Si le test post-coïtal est négatif (absence de spermatozoïdes dans la glaire), il faut chercher une lésion traumatique (traitement laser, conisation) ou infectieuse du col utérin.
Si les spermatozoïdes sont immobiles et le mucus de qualité correcte, on recherche des anticorps sériques chez la femme (laboratoire spécialisé) ou chez l’homme. Après un test de dépistage immunologique (test MAR) sur le spermogramme, on effectue un typage des anticorps anti-spermatozoïdes.
Si les spermatozoïdes sont peu mobiles, il peut s’agir d’une anomalie de la qualité du mucus ou du sperme. On effectue donc un test croisé d’interaction sperme-mucus in vitro : étude du sperme dans le mucus de la partenaire et dans une glaire témoin, et étude du mucus de la partenaire avec le sperme du partenaire et un sperme témoin.
Le traitement d’une infection du mucus permet parfois l’obtention de la grossesse. Sinon, on pratique des inséminations intra-utérines, si la qualité du sperme le permet.
4/5