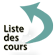3 - Étiologies
A. États d’hypogonadisme (hors ménopause)
La carence estrogénique provoque une augmentation de l’ostéoclastogenèse et l’activation des ostéoclastes, qui augmentent la résorption osseuse et donc la perte osseuse. La gravité de l’atteinte osseuse dépend de l’intensité et de la durée de l’hypogonadisme. Elle est d’autant plus marquée que l’hypogonadisme survient précocement, au cours de la période pubertaire, période d’acquisition du capital osseux. De plus, la présence d’autres facteurs de déminéralisation, telles les carences nutritionnelles, contribue à aggraver l’atteinte osseuse de certains hypogonadismes.
1. Anorexie mentale
a. Physiopathologie de l’atteinte osseuse
Il s’agit d’une ostéoporose à bas niveau de remodelage. Les marqueurs biochimiques de la formation osseuse (iso-enzyme des phosphatases alcalines, ostéocalcine) sont le plus souvent diminués. Les marqueurs de la résorption (CTx, NTx) sont normaux, parfois élevés (figure 8.1).
L’origine de l’ostéoporose est multifactorielle : la carence œstrogénique reste le principal facteur de perte osseuse, mais les troubles nutritionnels entraînant une carence calcique, une hypoprotidémie, une diminution de l’IGF1 et la sécrétion de leptine (diminution de la masse grasse) jouent un rôle aggravant. Un hypercortisolisme est également souvent retrouvé malgré l’absence de signes cliniques.
b. Masse osseuse et risque fracturaire
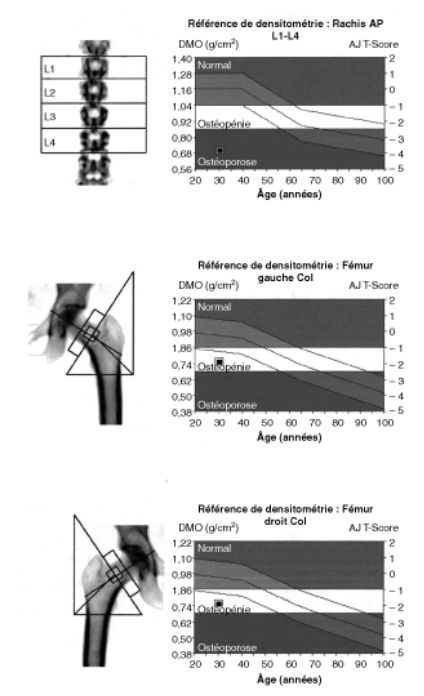
L’ostéoporose est fréquente dans l’anorexie mentale. Une ostéopénie (T-score compris entre – 1 et – 2,5) est retrouvée dans 50 à 95 % des cas, et une ostéoporose (T-score < – 2,5) dans 25 à 40 % des cas, selon les séries (figure 8.2). Le risque de fracture est globalement multiplié par 7 avec des fractures du col du fémur même chez de très jeunes femmes. L’atteinte osseuse est d’autant plus importante qu’elle survient chez un sujet jeune. De même, l’importance du déficit nutritionnel et la persistance d’un faible poids corporel sont des critères de gravité.
Déminéralisation osseuse prédominant au rachis (T score au niveau L1-L4 : 3,9).
c. Prévention et traitement
La substitution œstrogénique, parfois difficile à faire accepter, doit être envisagée le plus rapidement possible lorsque le diagnostic est établi. Cette œstrogénisation n’a cependant qu’un effet limité sur la DMO mais permet de limiter la perte osseuse. Le gain pondéral n’est associé à une amélioration de la DMO que s’il permet un retour des cycles menstruels spontanés. En cas de persistance de l’aménorrhée, la prise en charge nutritionnelle, de même que l’apport calcique n’ont que peu d’impact sur le niveau de la DMO. Des essais thérapeutiques récents avec des bisphosphonates (risédronate, alendronate) ont permis de montrer des gains significatifs de l’ordre de 4 à 5 % au terme de 9 à 12 mois de traitement.
2. Activité physique intensive
a. Physiopathologie de l’atteinte osseuse
Les femmes sportives soumises à une activité physique trop intense peuvent développer une hypoestrogénie d’origine hypothalamique (cf. chapitre 19 : « Aménorrhée »). Les facteurs retrouvés dans l’anorexie mentale (hyperactivité, conduites alimentaires restrictives) sont souvent présents.
Les facteurs conditionnant l’atteinte osseuse sont :
- le type et l’importance de l’activité sportive : marathon, danse classique (jusqu’à 60 % d’aménorrhée), demi-fond, triathlon, gymnastique, cyclisme (alors que la natation et les sports collectifs sont moins en cause) ;
- l’importance et la fréquence des troubles du cycle menstruel ;
- des apports alimentaires réduits ou insuffisants.
b. Masse osseuse et risque fracturaire
L’atteinte osseuse est de répartition inégale du fait de l’intrication des facteurs endocriniens et mécaniques sur le remodelage osseux. Les contraintes mécaniques stimulent l’ostéoformation sur des sites porteurs ; à l’inverse, l’hypoestrogénie est responsable d’une résorption osseuse généralisée, bien qu’à prédominance rachidienne. Il existe également une plus grande fréquence des fractures de fatigue, qui sont favorisées par la diminution de la DMO. L’ostéoporose est parfois sévère et multifracturaire, conduisant à l’arrêt des activités sportives. Elle apparaît réversible avec le retour à la reprise spontanée des cycles menstruels, souvent lors de la réduction de l’activité physique.
c. Prévention et traitement
Il est nécessaire d’informer l’athlète de l’impact potentiel des troubles du cycle sur le squelette. Si une aménorrhée s’installe et si la diminution de l’activité physique n’est pas possible, la mise en route d’un traitement par les estroprogestatifs représente une solution de choix. L’athlète doit également être sensibilisé vis-à-vis des déséquilibres nutritionnels et de l’importance de lutter contre les carences d’apport.
3. Pathologies hypophysaires
Toute lésion hypophysaire (tumorale, infiltrante, iatrogène, traumatique, etc.) provoquant une atteinte (réversible ou irréversible) de la fonction gonadotrope peut avoir des conséquences osseuses. Les hyperprolactinémies, d’origine tumorale (micro et macroprolactinomes) ou fonctionnelle, représentent les causes les plus fréquentes d’aménorrhée hypophysaire.
a. Physiopathologie de l’atteinte osseuse
La perte osseuse est liée à l’hyperactivité ostéoclastique, secondaire à la carence estrogénique, et sera variable en fonction de l’intensité et de la durée de l’hypoestrogénie. En dehors de leur impact sur l’axe gonadotrope, les atteintes hypophysaires, et en particulier les tumeurs hypophysaires autres que les prolactinomes (adénomes gonadotropes, à hormone de croissance, adénomes non sécrétants, etc.), n’ont pas d’impact propre sur le remodelage osseux (à l’exception des adénomes corticotropes dont l’impact osseux est secondaire à l’hypercortisolisme : maladie de Cushing) (voir item 220 « Adénome hypophysaire ».
b. Masse osseuse et risque fracturaire
Au plan clinique, l’installation d’une aménorrhée doit conduire à évaluer l’impact osseux qui concerne surtout l’os trabéculaire (rachis dorso-lombaire). La perte osseuse est souvent rapide, de l’ordre de 5 à 8 % par an, d’autant que l’hypogonadisme survient chez une femme jeune. Les possibilités de récupération osseuse sont très variables en fonction des capacités de récupération de l’axe gonadotrope (reprise spontanée des cycles menstruels), de l’étiologie de l’atteinte hypophysaire, de la durée de l’aménorrhée, de l’âge et du statut osseux antérieur.
c. Prévention et traitement
La prévention de la perte osseuse est fonction de la réversibilité prévisible de la pathologie hypophysaire (correction de l’hyperprolactinémie, notamment), de la durée antérieure de l’aménorrhée, de l’âge et du statut osseux sous-jacent. Chez les femmes non ménopausées, l’estrogénothérapie sera privilégiée en première intention et sous réserve des contre-indications classiques. En cas de contre-indication au traitement hormonal, un autre traitement (bisphosphonates, SERM, ranelate de strontium) sera discuté en fonction de l’importance du risque fracturaire. Les premiers résultats du denosumab, un anticorps monoclonal humain anti-RANKL, chez les femmes traitées par inhibiteur de l’aromatase et les hommes traités pour un cancer prostatique, sont très encourageants.
4. Hypogonadismes iatrogènes
Tous les traitements diminuant la production des estrogènes (ou des androgènes chez l’homme) constituent des facteurs potentiels d’augmentation du risque fracturaire. C’est le cas des agonistes du GnRH, utilisés dans le cadre de pathologies utérines (endométriose, fibromes) ou prostatiques, et des inhibiteurs de l’aromatase, nouveaux agents thérapeutiques du cancer du sein. Une mesure de la DMO peut être préconisée avant ces traitements, la perte osseuse pouvant être rapide, pour permettre une prévention adaptée en fonction du niveau de risque.
5. Dysgénésies gonadiques
Le syndrome de Turner est la dysgénésie gonadique féminine la plus fréquente, sa prévalence étant de l’ordre de 1 pour 2 500 filles à la naissance (chapitre « aménorrhée »).
a. Masse osseuse et risque fracturaire
Une diminution de la DMO est fréquente dans le syndrome de Turner, mais elle peut être liée en partie à la petite taille des pièces osseuses. Chez l’enfant en période prépubertaire, la densité minérale osseuse mesurée par DEXA apparaît normale lorsque la valeur est corrigée par la taille staturale. Il existerait néanmoins une diminution de plus de 1,5 écart types de la densité osseuse mesurée par scanner dans 15 à 20 % des cas, sans qu’il soit possible de déterminer s’il s’agit d’un trait phénotypique du syndrome de Turner ou du retentissement de l’hypoestrogénie prépubertaire. Au cours de l’adolescence, le déficit osseux apparaît s’accentuer du fait de l’hypogonadisme avec une augmentation du remodelage osseux, secondaire à la carence estrogénique. Chez l’adulte non traité, l’insuffisance ovarienne accentue la perte osseuse et il existe une augmentation du risque de fracture.
b. Prévention et traitement
Le traitement est avant tout fondé sur la correction de l’hypogonadisme, et l’estrogénisation est proposée dès que le diagnostic est posé, actuellement le plus souvent en association avec un traitement à l’hormone de croissance de manière à améliorer le pronostic statural. À l’âge adulte, la poursuite d’un traitement estroprogestatif permet la prévention de la perte osseuse.