- Pré-requis et Objectifs
-
Cours
-
Contenu
- 1 - Introduction et définitions
- 2 - Construction d’un diagramme de phases
- 3 - Diagrammes de phases avec miscibilité totale à l’état solide
- 4 - Diagrammes de phases avec miscibilité partielle à l’état solide
- Version Enseignants
-
Version PDF

-
Contenu
- Annexes
- Votre Avis
- Ressources Enseignants
4 - Diagrammes de phases avec miscibilité partielle à l’état solide
C’est évidemment le cas le plus fréquent dans les alliages binaires. Deux types de transformations peuvent se rencontrer : les diagrammes avec point eutectique et les diagrammes avec point péritectique.
4 . 1 - Diagrammes avec point eutectique
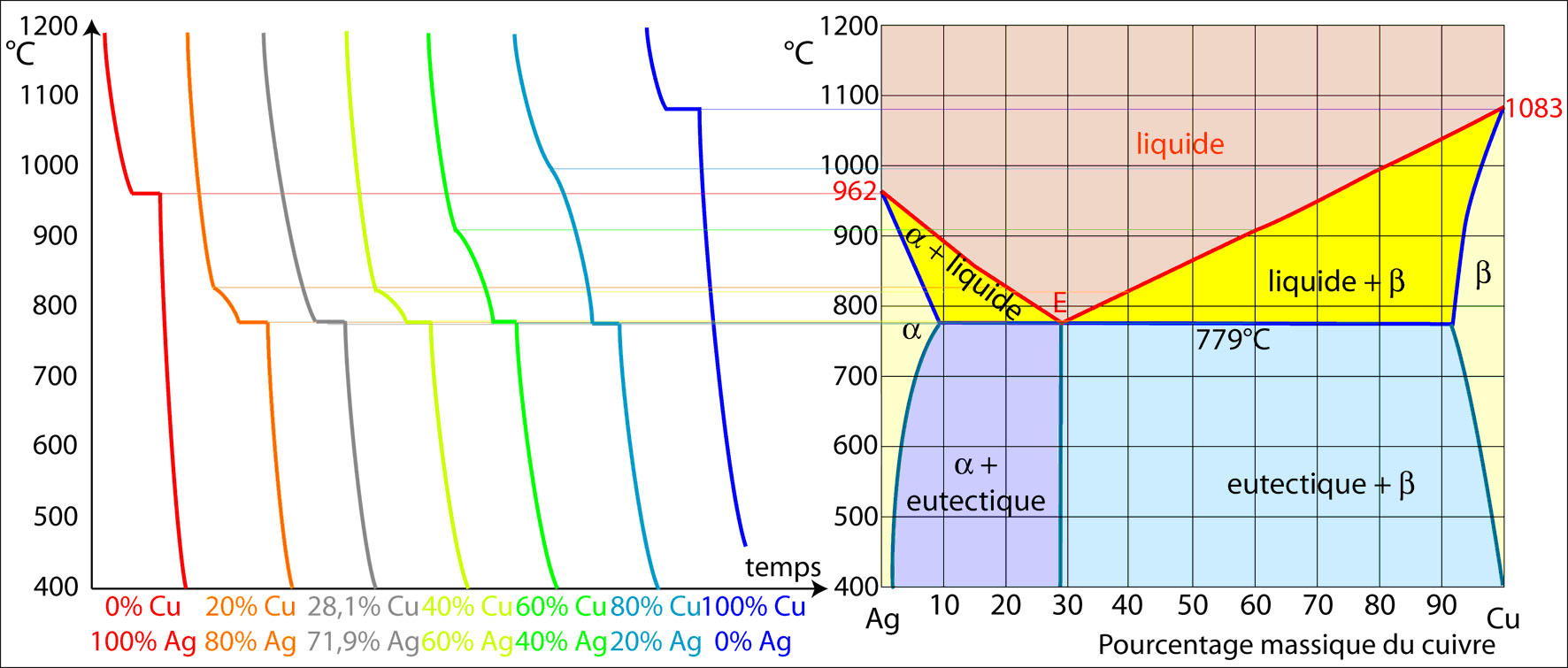
Dans ce type de diagramme existe un point invariant dont la température est inférieure à la température de fusion des deux constituants. Un des intérêts de ces alliages eutectiques et de pouvoir être utilisé en brasure. L’exemple présenté ici est l’alliage binaire argent-cuivre. Les températures de fusion de l’argent et du cuivre purs sont respectivement de 962°C et de 1083°C. À 779°C, la solubilité du cuivre dans l’argent est de 8,8% massique et la solubilité de l’argent dans le cuivre est de 8% massique. Pour les alliages compris entre ces deux intervalles, l’ensemble des courbes de refroidissement présente un palier isotherme dont la longueur maximale se situe au point eutectique (figure 7 : point E situé à 779°C avec 60,1% d’argent et 39,9% de cuivre).
Au niveau du point E ou point eutectique, l’équilibre s’établit entre trois phases : une phase liquide d’une part, et deux phases solides d’autre part. À ce point, un liquide se transforme simultanément en deux phases solides :
LE ⇔ α + ß
Les alliages situé à gauche du point eutectique s’appelle des alliages hypo-eutectiques et ceux situés à la droite des alliages hyper-eutectiques. Cette appellation est purement conventionnelle et dépend évidemment de l’orientation du diagramme de phase.
Figure 7 : construction d’un diagramme de phases avec point eutectique
La solubilité du cuivre dans l’argent, maximale à 779°C, diminue rapidement avec la baisse de la température. Cette transformation à l’état solide d’une phase a en deux phases α + eutectique se forme par précipitation d’une deuxième phase β avec la baisse de la température. La ligne séparant ces deux zones du diagramme s’appelle le solvus.
4 . 2 - Aspect micrographique de la phase a ou de la phase b
En microscopie métallographique, l’aspect après solidification est identique avec des grains de composition homogène à celui des alliages de constituants totalement miscibles.
4 . 2 . 1 - Aspect micrographique de l’alliage eutectique
Si la composition est rigoureusement celle de l’alliage eutectique, ici à 39,9% atomique de cuivre dans l’alliage argent-cuivre, nous obtenons un agrégat de grains semblables mais tous d’aspect hétérogène (figure 8).
En fonction des composants, l’aspect d’un eutectique peut présenter différentes morphologies, en lamelles, en batonnets, en globules ou aciculaire.
Le mécanisme de formation peut être expliquer de la façon suivante :
Les deux composants, le solvant et le soluté ne sont pas miscibles dans les proportions eutectiques. Un premier germe de cristallisation va se former à l’interface du liquide. Ce germe peut être par exemple du type a soit très riche en argent (85,9%at.). Pour atteindre cette concentration, il va rejeter le cuivre en excès dans son voisinage immédiat. Ce cuivre va à son tour se solidifier en phase β (cuivre : 95,1%at.) et rejeter alors l’argent en excès. Cet argent forme une nouvelle couche α… Cette succession alternée de solidification de deux types cristallins différents donne cet aspect caractéristique des alliages eutectiques.
Figure 8 : aspect d’un alliage eutectique
6/8