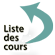L’ion Na+ est plus petit que l’ion Cl-. Il faut que l’ensemble du cristal reste électriquement neutre, il y a donc un ion Na+ pour un ion Cl- et le centre de la maille est occupé par un ion Na+.
Retour au cours
Figure 20 : Structure cristalline du NaCl – Structure cubique face centrée (CFC)
Retour au cours
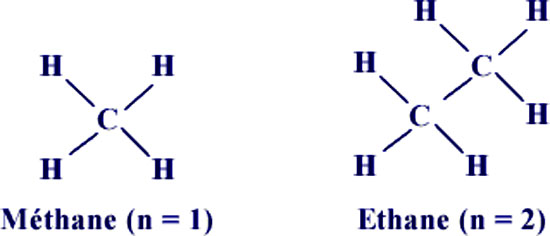
Figure 21 : Les deux 1ers membres de la famille des alkanes : le méthane (n=1) et l’éthane (n = 2)
Retour au cours
Figure 23 : Exemples de défauts ponctuels dans les solides cristallins