- Pré-requis et Objectifs
-
Cours
-
Contenu
- 1 - Définition et mécanisme des infections nosocomiales
- 2 - Antiseptiques
- 3 - Protocoles de soins
-
4 - Stérilisation : techniques et controles
- 4.1 - Processus autour de la stérilisation
- 4.2 - Moyens de stérilisation
-
4.3 - Contrôles de stérilisation
- 4 . 3 . 1 - Contrôles physiques (autoclave)
- 4 . 3 . 2 - Contrôles chimiques : contrôle de pénétration de la vapeur, test de Bowie et Dick
- 4 . 3 . 3 - Contrôles chimiques : indicateurs de passage
- 4 . 3 . 4 - Contrôles chimiques : tests colorimétriques
- 4 . 3 . 5 - Contrôles chimiques : les intégrateurs
- 4 . 3 . 6 - Contrôles batériologiques
- 5 - Elimination des dechets
- 6 - Organismes et comissions, legislation
-
7 - Architecture et locaux
-
7.1 - Quelques rappels historiques
- 7 . 1 . 1 - Epoque médiévale
- 7 . 1 . 2 - Hôpital en croix de la Renaissance et époque classique
- 7 . 1 . 3 - Hôpital hygiéniste : architecture ventilée de la fin du 18eme siècle
- 7 . 1 . 4 - L’hôpital pavillonnaire de la fin du 19eme Siècle
- 7 . 1 . 5 - L’hôpital Monobloc : symbole de la médecine triomphante
- 7 . 1 . 6 - L’hôpital polybloc ouvert sur la ville
- 7.2 - Nettoyage des locaux et surfaces
-
7.1 - Quelques rappels historiques
- 8 - Bibliographie
- Version Enseignants
-
Version PDF

-
Contenu
- Annexes
- Votre Avis
- Ressources Enseignants
4 - Stérilisation : techniques et controles
4 . 1 - Processus autour de la stérilisation
4 . 1 . 1 - Décontamination (ou pré-désinfection) et désinfection
La décontamination est le premier traitement à effectuer sur les objets et matériels souillés dans le but de diminuer la population de micro-organismes et de faciliter le nettoyage ultérieur.
Pratiquée d’emblée, elle vise tout d’abord à éliminer les souillures visibles et comporte l’essuyage externe avec des compresses ou du papier à usage unique et +/- le rinçage abondant à l’eau du réseau.
La pré-désinfection a également pour but de protéger le personnel lors de la manipulation des instruments et d’éviter la contamination de l’environnement.
C’est l’étape indispensable avant toute désinfection ou stérilisation.
La désinfection est une opération au résultat momentané, qui permet d’éliminer ou de tuer les microorganismes et/ou d’inactiver les virus indésirables portés par les milieux inertes contaminés en fonction des objectifs fixés. Le résultat de cette opération est limité aux micro-organismes présents au moment de l’opération.
Lors d’une désinfection, il n’y a pas de conditionnement de l’objet, et dès la fin du traitement une recolonisation de l’objet survient. Par définition, une désinfection vise à réduire une population de micro- organismes, mais pas nécessairement à la supprimer en totalité. Selon la norme AFNOR, un désinfectant doit permettre d’obtenir une réduction d’un inoculum bactérien de 5 log., d’un inoculum de champignon de 4 log.,d’un inoculum viral de 4 log. et d’un inoculum de spores de 5 log. Aussi et après désinfection, un objet peut-il être encore porteur de micro-organismes si l’inoculum de départ est élevé.
Par ailleurs, lors d’une désinfection, il n’existe pas de méthode permettant la validation du cycle de désinfection.
Trempage :
Les produits utilisés peuvent posséder uniquement des propriétés de détergence (détergent) ou combiner des propriétés de détergence et de désinfection (détergent-désinfectant), cette combinaison étant la plus fréquente. Si le produit est un détergent-désinfectant, il ne doit pas contenir d’aldéhyde et doit posséder les qualités suivantes :
- bactéricide selon la norme AFNOR NF T 72-150 ou 72-151 spectre 5.
- fongicide selon la norme AFNOR NF T 72-200 ou 72-201, sinon au minimum être efficace vis-à-vis de Candida albicans selon la norme AFNOR NF T 72-300 ou 72-301.
- virucide selon la norme AFNOR NF T 72-180, sinon être au minimum efficace sur le virus VIH.
- bactéricidie selon la norme AFNOR NF T 72-170 ou 72-171 spectre 5 en condition de saleté (et en présence d’eau dure selon la dureté de l’eau du réseau si le produit est à diluer).
Il n’existe pas actuellement de méthode normalisée qui permette d’apprécier et de comparer les capacités de détergence d’une formulation.
Après trempage, le matériel sera brossé, nettoyé, puis rincé abondamment à l'eau du réseau. Pour ce faire, le personnel affecté à cette tâche, revêtu de gants longs et épais, ouvrira les articulations des instruments afin d'éviter toute zone d'ombre néfaste à un bon nettoyage. Pendant cette opération, il devra porter également des lunettes de protection qui seront désinfectées aussi souvent que nécessaire et au moins une fois par jour et un tablier plastique à usage unique.
Le bain de détergent-désinfectant (dD) sera changé aussi souvent que possible, et au bloc opératoire après chaque intervention. Les bacs de trempage seront nettoyés et désinfectés tous les jours à la fin de l'activité opératoire.
L'utilisation de machines à laver et à désinfecter les instruments avec un cycle détergent et une montée thermique (80° et plus), permet de supprimer cette phase de trempage à condition de mettre les instruments immédiatement dans la machine : la machine se trouve à côté du bloc et les instruments sont mis directement dans les paniers.
Il existe des appareils à ultra-sons, qui ne désinfectent pas, mais qui sont particulièrement intéressants pour décoller les souillures sur les pinces à biopsie et autres instruments délicats et difficiles à nettoyer. Ils seront remplis avec une solution dD pour faire tremper les instruments.
Le matériel lavé sera examiné sérieusement avant le conditionnement : il serait effectivement aberrant de stériliser des instruments non utilisables ultérieurement.
Pour le matériel médico-chirurgical, il faut distinguer le matériel à usage unique d'une part, et le matériel réutilisable d'autre part.
Le nettoyage :
Le nettoyage des instruments fait suite à l’opération de pré-désinfection. Tout nettoyage associe un agent chimique détergent et un agent physique.
Dans tous les cas, le nettoyage au moyen d’une machine à laver est préférable au nettoyage manuel.
Le lavage manuel dans un bain de cette même solution détergente, doit comporter en particulier le brossage des extrémités, des recoins et anfractuosités, et l’écouvillonnage des canaux. Le rinçage se fait à l’eau du réseau.
Le séchage :
Il est réalisé en fin de nettoyage.
Après cette première phase, on peut envisager trois possibilités selon l'usage du matériel ou la composition du matériau le constituant. En effet :
- soit le matériel doit être propre : dans ce cas, on peut se contenter de cette phase de nettoyage-désinfection dans un produit dD et le produit sera rangé dans le lieu de stockage adéquat.
- soit il doit être stérile, mais il est thermosensible : il subira donc une désinfection à basse température, soit chimique à l'aide du glutaraldéhyde, soit par gaz plasma ou oxyde d'éthylène.
- soit il doit être stérile, mais il est thermostable : il sera stérilisé par la chaleur humide (autoclave vapeur)
Ces étapes du processus de stérilisation sont primordiales car "ON NE STERILISE BIEN QUE CE QUI EST PROPRE ET SEC ".
4 . 1 . 2 - Stérilisation
La stérilisation est une opération permettant d’éliminer ou de tuer les micro-organismes portés par des milieux inertes contaminés, le résultat de cette opération ayant pour objectif le degré 0 en fin d'opération.(= le produit est stérile) et permettant de conserver cet état pour une période de temps précisée.
Sur un objet stérile au contraire, la survie de micro-organismes est hautement improbable et le conditionnement permet de conserver la stérilité durant un certain temps.
Lors d’une stérilisation correctement menée, il existe une assurance de ne pas retrouver plus d’un micro-organisme vivant par 15.106 unités soumises à la stérilisation. Selon la norme Européenne, lorsqu’un objet est étiqueté stérile, la probabilité théorique qu’un micro-organisme viable soit présent sur un dispositif doit être à 1 pour 106. En d’autres termes, on ne doit pas retrouver plus d’un objet contaminé sur 1 million.
La stérilisation est par ailleurs une méthode qui s’accompagne de contrôles permettant de valider un cycle de stérilisation.
Il faut donc être bien conscient qu’une désinfection n’apporte pas le même niveau de sécurité qu’une stérilisation.
LA RESTERILISATION DU MATERIEL A USAGE UNIQUE EST INTERDITE.
La stérilisation proprement dite :
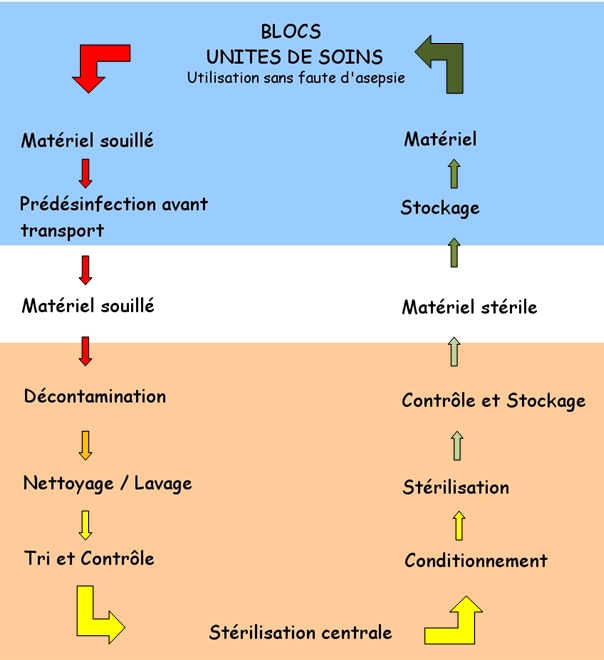
La mise en oeuvre d’un ensemble de méthodes et de moyens visant à éliminer (destruction) tous les micro-organismes vivants de quelque nature et sous quelque forme que ce soit, portés par un objet parfaitement nettoyé.
Figure 1 : Représentation schématique de la stérilisation
Le conditionnement :
Quel que soit le conditionnement choisi, il doit présenter les qualités suivantes :
- Maintenir avant stérilisation le niveau minimum de contamination initiale obtenu par le nettoyage.
- Permettre le contact avec l’agent stérilisant ; le choix du conditionnement dépendra donc du mode de stérilisation envisagé.
- Assurer le maintien de la stérilité jusqu’au moment de l’utilisation.
- Participer au maintien de l’intégrité des caractéristiques organoleptiques, physiques, chimiques et mécaniques du matériel.
- Permettre l’extraction et l’utilisation de ce matériel dans des conditions aseptiques.
Il se réalise selon différentes modalités : containers+/- paniers, sachets, feuille de papier crêpé et feuilles en non tissé.
4 . 2 - Moyens de stérilisation
4 . 2 . 1 - Stérilisation par la chaleur pour les instruments qui résistent à la chaleur
Stérilisation par la chaleur sèche
Elle est de moins en moins utilisée : Poupinel.
Appareil peu fiable ne permettant de toute façon que de traiter du verre et du métal qui a disparu ou quasiment en milieu hospitalier.
Les températures utilisées doivent être élevées : 180°, 1H30.
Stérilisation par la chaleur humide (Autoclave)
Le premier stérilisateur à vapeur à usage hospitalier a vu le jour en 1881, il s'agissait alors d'un stérilisateur portable de 6 litres, chauffé à l'alcool.
La stérilisation par la vapeur d'eau est le procédé de référence pour la stérilisation en milieu hospitalier.
L'autoclave est un appareil à pression de vapeur d'eau.
L'action conjuguée de la vapeur d'eau et de la température (température supérieure à 120°C) provoque la dénaturation puis la mort des micro-organismes (bactéries, virus,…) présents sur ou dans le matériel (y compris les Agents Toxiques Non Contaminant, ou ATNC, comme le prion, si un cycle spécifique est réalisé).
Principes de fonctionnement
L'autoclave fonctionne selon un "cycle de stérilisation" qui comporte les étapes suivantes :
- le préchauffage de l'enceinte et de ses parois, qui évite la condensation de vapeur au niveau de la charge qui sinon risquerait de sortir humide en fin de cycle,
- la purge de l'appareil et la réalisation du vide pour chasser l'air de l'enceinte (très mauvais conducteur de chaleur) et pour obtenir des vapeurs saturantes,
- la montée en température et en pression de la vapeur d'eau,
- la stérilisation qui commence lorsque la température et la pression choisies sont atteintes et s'achève lorsque celles-ci diminuent,
- le séchage par le vide qui permet d'évacuer la vapeur d'eau,
- le retour à la pression atmosphérique pour permettre l'ouverture de la porte.
En pratique, les temps de stérilisation minimum à respecter sont : 20 min de phase de stérilisation à 121°C ; 15 min à 126°C ; 10 min à 134°C.
Un certain nombre d'appareils sont intégrés à l'autoclave :
- thermomètre (mesure de la température de l'enceinte) : il doit être visible et lisible,
- manomètre (mesure de la pression dans l'enceinte),
- régulateur de température, manovacuomètre enregistreur : présent sur certains modèles d'autoclave, il enregistre et restitue sous la forme d'un tracé les différentes phases d'un cycle de stérilisation. Il fonctionne de façon électrique ou mécanique.
Il existe plusieurs types d'enregistrement :
- à disque (diagramme circulaire, une voie d'enregistrement : pression)
- à déroulement linéaire (ticket, deux ou trois voies d'enregistrement : vide, pression, température). De plus, le quadrillage du papier permet le minutage.
On doit toujours stériliser à la vapeur d'eau ce qui peut l'être, en particulier : textiles, pansements (tissé et non-tissé), instruments chirurgicaux en acier inox, verrerie, caoutchouc, certains plastiques.
Inconvénients :
Face à la médecine moderne, la stérilisation à la vapeur connaît des limites : de nombreux instruments, souvent coûteux, ne peuvent être stérilisés à l'autoclave, à cause de leur sensibilité à la chaleur.
4 . 2 . 2 - Stérilisation par les gaz ou les radiations ionisantes pour les instruments qui ne résistent pas à la chaleur
La stérilisation par l’oxyde d’éthylène : c’est un gaz très utile pour stériliser le matériel médicochirugical thermosensible.
Peu implantée en France dans le milieu hospitalier, malgré un bon compromis entre le coût et la praticabilité. Malgré sa fiabilité (gaz bactéricide, fongicide, virucide et sporicide), cette technique présente un certain nombre d’inconvénients dont son caractère toxique pour le personnel et le malade et ses propriétés inflammables. Les instruments stérilisés par une telle méthode doivent faire l’objet d’une désorption de plusieurs heures, limitant la disponibilité du matériel ainsi traité.
Le personnel utilisant ce type de matériel doit être particulièrement formé et informé des risques de ce procédé tant pour leur sécurité que pour celle des malades. Seule une installation en stérilisation centrale est autorisée : l'oxyde d'éthylène est un gaz toxique, inodore, dont on ne perçoit pas la présence dans l'air.
Il est toxique:
- par inhalation (irritation respiratoire et dépression du système nerveux central)
- par contact (réactions irritatives de la peau et des muqueuses)
- par voie parentérale (phénomènes hémolytiques, sténoses trachéales, collapsus cardio-vasculaires et phénomènes allergiques)
- par réaction avec différents corps chimiques: produits toxiques.
UNE PERIODE DE DESORPTIONDéfinitionest la transformation inverse de la sorption, par laquelle les molécules sorbées se détachent du substrat. Par exemple la désorption thermiques est l’incinération. Le séchage et l’essorage sont aussi des formes de désorption. EST INDISPENSABLE (au moins 3 semaines =>prévoir la stérilisation longtemps à l'avance)
La stérilisation à l'oxyde d'éthylène doit être réservée au matériel thermosensible, qui ne peut pas être stérilisé autrement
- plastiques ne supportant pas la chaleur, et dont on connaît le temps de désorption.
- instruments à matériaux composites qui seraient détériorés par la stérilisation à la vapeur.
- matériaux fragiles (photos, effets personnels neufs pour malades en chambre stérile)
La stérilisation par le formaldéhyde gazeux : c’est un agent de stérilisation en surface, ne pénétrant pas en profondeur à l’inverse de l’oxyde d’éthylène.
Il est de plus corrosif et sa désorption se poursuit après stérilisation.
Il faut rappeler à ce propos que l’utilisation de pastilles de trioxyméthylène comme moyen de stérilisation doit être bannie car non contrôlable, inefficace et nocive.
La stérilisation par gaz plasma de peroxyde d'hydrogène représente très certainement une voie d’avenir très prometteuse dans les techniques de stérilisation des dispositifs médicaux réutilisables et thermosensibles.
Cet appareil (Sterrad 100) utilise la vapeur de peroxyde d’hydrogène introduite dans un récipient sous vide (dépression < 20mmHg) qui va être excitée par une onde électromagnétique, induite par une onde radio.
Avantages :
- permet de stériliser à basse température (45°)
- utilisation simple et non toxique
- cycle rapide (75 mn)
- ne nécessite pas de désorption
Inconvénients :
- coûteux
- ne permet pas de traiter les objets comportant de la cellulose : les emballages devront être non en papier, mais en matières plastiques ou non tissé.
- ne permet pas de traiter les instruments de masse importante, ni les liquides
- la stérilisation par les radiations ionisantes, en particulier par les rayons gamma, présente de nombreux avantages (utilisation sur du matériel thermosensible, absence de risque d’irradiation résiduelle), mais cette technique n’est pas actuellement utilisée en milieu hospitalier.
C'est une installation très lourde, très coûteuse, donc peu répandue.
Concerne essentiellement le matériel médico-chirurgical à usage unique.
4 . 2 . 3 - Stérilisation à froid du matériel thermosensible (endoscopes)
Le Glutaraldéhyde in vitro inactive :
- herpès et poliovirus en 1 minute
- HIV en 2 minutes
- bactéries en 5 minutes (sauf mycobactéries)
- virus de l'hépatite B en 10 minutes
- champignons en 15 minutes
- BK en 20 minutes
- spores entre 1 et 10 heures selon fournisseurs et produits.
Il faut rincer à l'eau stérile immédiatement avant utilisation.
4 . 3 - Contrôles de stérilisation
QUEL QUE SOIT LE PROCEDE UTILISE, IL FERA L'OBJET DE CONTROLES.
4 . 3 . 1 - Contrôles physiques (autoclave)
Vérifications des paramètres physiques sur les diagrammes (linéaires ou circulaires) qui enregistrent : la montée de la température, le temps, la pression, au cours des cycles de stérilisation
L’archivage des diagrammes est obligatoire (traçabilité).
4 . 3 . 2 - Contrôles chimiques : contrôle de pénétration de la vapeur, test de Bowie et Dick
Test fondamental pour la surveillance du bon fonctionnement de l'autoclave, à effectuer tous les matins lors de la mise en route des appareils, et après toute opération de maintenance. Constitue également un test d'absence d'air résiduel ou de rentrée d'air au vide du stérilisateur.
En pratique,:
un paquet standard d'environ 25 cm de côté et 27 cm de hauteur est constitué de 25 à 36 champs opératoires d'environ 1 m de côté, lavés et aérés, pliés sur eux-mêmes plusieurs fois. Au milieu de la pile, on place une feuille de papier blanc non glacé, sur laquelle est tracée une croix en papier adhésif portant une encre qui ne doit virer qu'après trois minutes de contact avec la vapeur à 134°C. La pile de tissu, attachée avec du ruban adhésif, est placée seule dans l'autoclave, et traitée à 134°C pendant un maximum de 3,5 minutes.
Interprétation du test de Bowie et Dick: à la sortie de l'autoclave, on examine la feuille au niveau de la croix :
Si la pénétration de la vapeur est rapide et complète, le virage de l'encre est homogène.
S'il subsiste de l'air résiduel, le ruban montre une différence de couleur entre le centre et les bords.
Si le résultat du test n'est pas satisfaisant, le stérilisateur doit être considéré comme défectueux, car la température souhaitée ne sera pas atteinte au coeur de la charge.
4 . 3 . 3 - Contrôles chimiques : indicateurs de passage
Ils indiquent qu'un des facteurs de stérilisation (la température par exemple) a été atteint, mais ne prouvent pas l'obtention des autres facteurs nécessaires à une stérilisation efficace (la durée de contact par exemple)
Les tubes témoins contiennent une poudre colorée dont le point de fusion se situe à une température connue.
Les rubans, pastilles ou étiquettes adhésives sont impressionnés d'une encre spéciale qui vire à une température donnée. L'encre témoin utilisée varie selon le mode de stérilisation : chaleur séche ou humide, oxyde d'éthylène.
4 . 3 . 4 - Contrôles chimiques : tests colorimétriques
Ils prennent en compte deux paramètres.
Les tubes de Brown: utilisés pour la stérilisation à la chaleur sèche (points verts et bleus) ou la vapeur d'eau saturée sous pression (points noirs et jaunes). Ce sont des ampoules scellées dont le liquide vire progressivement, en fonction de la température et du temps de contact.
Les tests de Brown : pour la stérilisation au formaldéhyde. C'est un papier imprégné d'un réactif virant au violet en présence des vapeurs de formol, et qui est enfermé dans un sachet plastique dont la perméabilité fait intervenir le temps de contact.
4 . 3 . 5 - Contrôles chimiques : les intégrateurs
Les intégrateurs prennent en compte tous les paramètres : température, temps de contact, saturation en vapeur d'eau, et concentration en gaz pour la stérilisation à l'oxyde d'éthylène.
La courbe de lecture des réactions chimiques est parallèle à celle de la destruction des spores. Il existe:
- des cartes avec des spots qui changent de couleur graduellement et par séquence autonomes au fur et à mesure que les paramètres de stérilisation sont atteints.
- des réservoirs de cire colorée, scellés entre deux feuilles d'aluminium. En fonction des paramètres souhaités, la cire fond graduellement, visualisant la courbe d'efficacité de la stérilisation.
Tous ces tests sont archivés, soit en stérilisation centrale, soit dans les dossiers des patients (traçabilité).
4 . 3 . 6 - Contrôles batériologiques
Ils utilisent le degré de survie de certains spores non pathogènes. Il existe des tests:
- qui nécessitent le recours à un bactériologiste : ces tests doivent être adressés au laboratoire pour mise en culture sur un milieu approprié et observation des résultats quelques jours plus tard.
- qui ne nécessitent pas le recours au bactériologiste et sont prêts à l'emploi.
Puis stockage du matériel (verticalité, écritures sur le papier, etc...)
Stocker le matériel dans un endroit propre, sec, tempéré et à l'abri de la poussière; le ranger par catégories en évitant les entassements.
Le temps de validité de la stérilité du matériel varie selon le moyen et l'emballage utilisé :
4/8