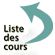2
-
Thrombose et maladie thrombo-embolique
2
.
1
-
Thrombose
La thrombose correspond à la coagulation du sang dans une cavité vasculaire (cœur, artère, veine, capillaire) au cours de la vie.
Le thrombus ainsi formé exclut par définition :
- les caillots sanguins formés après la mort (caillots post-mortem ou cadavériques) ;
- une collection de sang coagulé hors d’une cavité vasculaire (c’est un hématome).
2
.
1
.
1
-
Pathogénie de la formation du thrombus
Trois facteurs principaux, dont l’importance respective varie selon les situations pathologiques, interviennent dans la formation d’un thrombus. C’est la triade de Virchow (figure 4.5).
Facteur pariétal
Il s’agit d’une lésion de la paroi vasculaire aboutissant à une interruption de l’endothélium : elle permet le contact entre le sang et la matrice extra-cellulaire sous-endothéliale. Ce facteur est le seul qui soit nécessaire à la constitution d’une thrombose et qui soit suffisant à lui seul pour déclencher le processus thrombotique. Il est souvent isolé dans les thromboses artérielles et intracardiaques.
On inclut également dans les mécanismes pariétaux certaines conditions dans lesquelles il n’y a pas de véritable destruction endothéliale, mais une activation endothéliale pro-coagulante faisant perdre les propriétés de thrombo-résistance de l’endothélium (sous l’effet de toxines bactériennes, par exemple).
Les causes de cette lésion pariétale sont multiples :
- traumatismes : compression ou contusion vasculaire ;
- turbulences circulatoires : au niveau des valvules ou des carrefours vasculaires (rôle surtout dans la constitution des thromboses artérielles et intracardiaques) ;
- inflammation : artérites, phlébites, phénomènes septiques de voisinage ;
- athérosclérose.
Facteur hémodynamique
La stase (ralentissement de la circulation sanguine) est un facteur prédominant de la formation des thromboses veineuses. Elle entraîne également une souffrance endothéliale par hypoxie. Elle favorise surtout l’augmentation de taille d’une microthrombose déjà constituée.
Les causes de la stase sanguine sont nombreuses :
- veines : varices, décubitus prolongé, immobilisation plâtrée ;
- artères : anévrisme, hypotension.
Facteur sanguin
Le terme d’hypercoagulabilité regroupe l’ensemble des altérations des voies de la coagulation favorisant la thrombose. L’hypercoagulabilité est plus inconstamment impliquée dans la constitution des thromboses que les deux facteurs précédents, mais constitue un facteur de risque indéniable pour les patients qui en sont atteints. Parmi ses causes, on peut citer :
- les maladies de la coagulation sanguine proprement dites, génétiques ou acquises ;
- les états d’hyperviscosité sanguine (polyglobulie, hémoconcentration) ;
- la contraception orale, l’hypercholestérolémie.
2
.
1
.
2
-
Morphologie du thrombus
2
.
1
.
2
.
1
-
Le thrombus récent
Il peut prendre des aspects variables, qui dépendent de son siège et de ses circonstances d’apparition.
Dans le cœur et les artères : il apparaît en général au niveau d’une lésion endothéliale (plaque athéroscléreuse) ou d’une zone de turbulences (anévrisme). Il adhère à la paroi vasculaire au niveau de la lésion d’origine, et a tendance à s’étendre de façon rétrograde.
Dans le système veineux : il siège habituellement dans une zone de stase sanguine et a tendance à s’étendre en suivant le sens du flux sanguin.
Dans sa forme typique, le thrombus veineux, constitué après plusieurs heures, comporte trois parties, caractérisant le thrombus fibrino-cruorique :
-
une tête : le thrombus blanc constitué de plaquettes et de fibrine adhérant à la paroi ;
-
un corps : le thrombus mixte constitué en alternance d’éléments figurés du sang (leucocytes, hématies, plaquettes) et de fibrine : aspect hétérogène et strié (stries de Zahn). Le mécanisme de cette alternance est expliqué par les turbulences consécutives à l’obstacle initial (tête) : il se crée une série d’ondes stationnaires où le sang est immobile et coagule (bandes rouges), alternant avec des zones de turbulences, où les plaquettes et la fibrine s’accumulent (bandes blanches) favorisant la coagulation sanguine dans la bande rouge suivante ;
-
une queue : le thrombus rouge, formé de sang plus ou moins bien coagulé avec peu de fibrine, flottant vers l’aval du vaisseau, parfois sur plusieurs centimètres de long.
2
.
1
.
2
.
2
-
Le degré d’oblitération du conduit vasculaire est variable
-
Thrombus totalement oblitérant : il s’agit le plus souvent d’un thrombus veineux ou capillaire, mais aussi des thrombus des artères de petit ou moyen calibre.
-
Thrombus partiellement oblitérant ou mural : artères de gros et moyen calibre, cœur.
Macroscopiquement, le thrombus formé in vivo est ferme, adhérent à la paroi et sec. Ces caractéristiques permettent, lors de la réalisation d’une autopsie, de le distinguer de caillots constitués post-mortem. Ces derniers sont lisses, brillants, rouge sombre (« gelée de groseille ») ou jaunâtres, moulés sur les cavités vasculaires, non-adhérents.
2
.
1
.
2
.
3
-
Évolution anatomique du thrombus
Si le thrombus n’est pas responsable du décès immédiat, les différentes évolutions suivantes peuvent être observées.
Thrombolyse
C’est la destruction du thrombus par les enzymes fibrinolytiques du plasma, avec restauration de la perméabilité vasculaire. C’est en fait une éventualité rare mais qui peut être provoquée par la thérapeutique. Elle est surtout possible dans le cas de thrombus petits et récents.
Organisation du thrombus
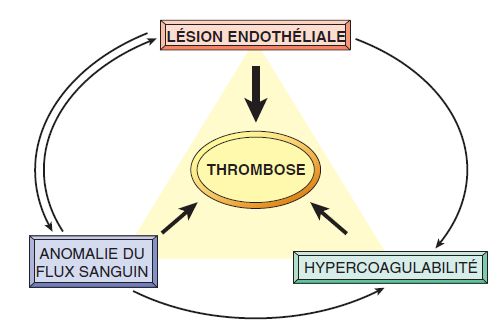
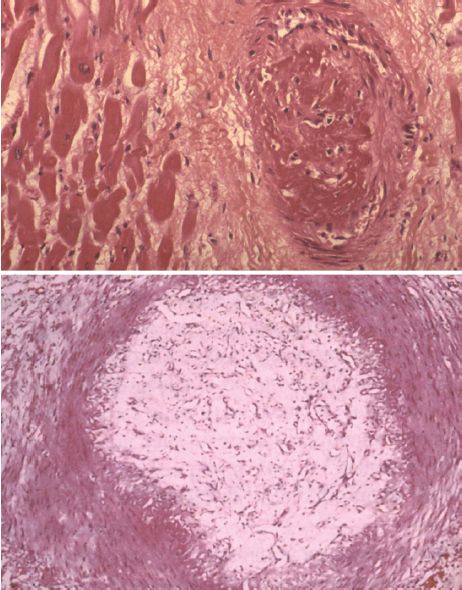
C’est l’éventualité la plus fréquente. Il s’agit d’une organisation fibreuse qui débute à la 48e heure. Le thrombus est progressivement recouvert et pénétré par des cellules endothéliales, par des monocytes-macrophages et par des cellules musculaires lisses, provenant de la paroi vasculaire à laquelle il adhère. Progressivement le thrombus est remplacé par un tissu conjonctif néo-formé qui apparaît à la zone d’insertion du thrombus et qui contient des fibres collagènes, des néo-capillaires sanguins et des macrophages chargés d’hémosidérine. Si le thrombus était mural, il va s’incorporer à la paroi vasculaire (épaissie) en se recouvrant progressivement de cellules endothéliales. Si le thrombus était oblitérant, les néo-vaisseaux sanguins qui traversent le thrombus peuvent aboutir à une reperméabilisation de la lumière vasculaire. Celle-ci reste le plus souvent incomplète ou très rudimentaire (figure 4.6). En l’absence de reperméabilisation, le thrombus organisé pourra éventuellement se calcifier (rare), aboutissant à la constitution de phlébolithes au niveau de varices thrombosées, par exemple.
Migration du thrombus (embolie)
Il s’agit de la rupture de tout ou partie du thrombus (surtout de la queue, non adhérente) avec migration dans le courant sanguin constituant un embole. Ce phénomène constitue le risque évolutif principal des thromboses, notamment des thromboses veineuses profondes, ainsi que des thromboses des artères de gros calibre comme l’aorte ou des thromboses intracardiaques. La rupture est surtout précoce, dans les heures suivant la formation du thrombus, avant le stade d’organisation fibreuse qui fixe plus solidement le thrombus à la paroi.
Ramollissement du thrombus
Il s’agit d’une évolution rare, qui résulte de l’action des enzymes des polynucléaires présents dans le thrombus. Le ramollissement peut survenir sur un thrombus récent aseptique, et favoriser sa migration. Le ramollissement purulent (suppuration) est rare. Il correspond à l’infection primitive (par exemple dans le cas d’une endocardite) ou secondaire du thrombus par des bactéries, avec risque de désintégration-migration du thrombus et d’embolie septique.
2
.
1
.
3
-
Formes topographiques des thromboses
Thromboses veineuses
Le principal facteur déclenchant est la stase. Le ralentissement du courant veineux s’observe dans toutes les conditions de décubitus prolongé. Il peut être majoré par des troubles de la tonicité de la paroi veineuse (varices), par un ralentissement du débit cardiaque (insuffisance cardiaque) ou par une compression veineuse. Il peut être associé à des atteintes de l’endothélium par des toxines (thromboses des foyers inflammatoires et infectieux).
Les localisations les plus fréquentes sont les veines du mollet et les branches profondes de la veine fémorale.
Les principales conséquences sont la stase locale (œdème et troubles trophiques tissulaires) et le risque d’embolie pulmonaire pour les thromboses des veines profondes.
Thromboses intracardiaques
Elles peuvent être déclenchées par une stase : thrombus dans l’oreillette gauche en amont d’un rétrécissement mitral, thrombose auriculaire dans les fibrillations auriculaires. On retrouve souvent un facteur pariétal causal :
- thrombus mural développé sur une zone d’infarctus du myocarde ;
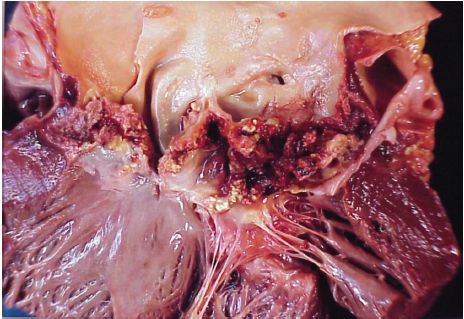
- thrombus sur les valvules cardiaques altérées par une infection bactérienne ; on appelle ces thrombus des « végétations » (figure 4.7) ;
- thrombose sur prothèse valvulaire.
Le principal risque évolutif est l’embolie.
Thromboses artérielles
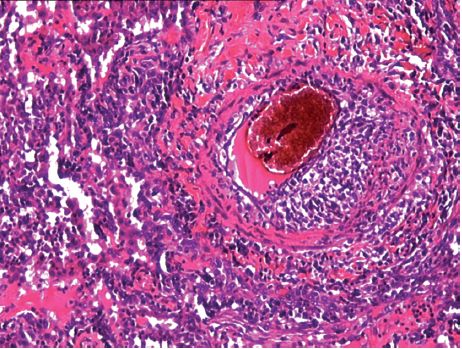
Elles sont essentiellement déclenchées par le facteur pariétal, c’est-à-dire l’altération de la paroi artérielle (au minimum l’altération du seul endothélium). La cause principale est l’athérosclérose. Moins fréquemment, elles peuvent être la conséquence d’atteintes inflammatoires primitives de la paroi artérielle (synonymes : artérite ou angéite [figure 4.8]) ou d’une déformation de la paroi (anévrisme).
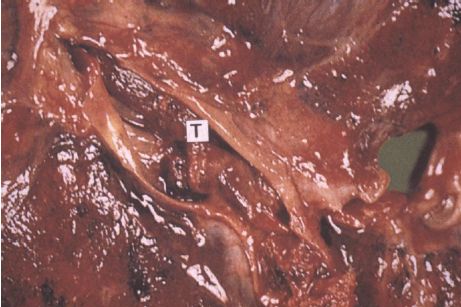
Les localisations les plus fréquentes correspondent aux artères les plus touchées par l’athérosclérose : aorte, artères des membres inférieurs, coronaires (figure 4.9), carotides, artères rénales, artères mésentériques, artères cérébrales.
Les principales conséquences sont l’ischémie locale et le risque d’embolie dans la grande circulation.
Thromboses capillaires
Elles sont favorisées par la stase et par les lésions endothéliales (anoxie, état de choc ou effet de toxines). Elles sont généralement multiples, à l’occasion du syndrome de coagulation intravasculaire disséminée (CIVD). Ce syndrome est caractérisé par la présence dans le lit vasculaire microcirculatoire de multiples thrombus fibrino-plaquettaires. Il est habituellement associé à un syndrome biologique de coagulopathie de consommation, avec pour conséquences des phénomènes hémorragiques diffus. Les étiologies d’une CIVD sont variées : septicémie à bactéries gram négatives, état de choc, embolie amniotique, traumatisme sévère, toxines (venins), etc. Elles siègent préférentiellement dans certains organes : poumons, glomérules rénaux, cerveau, foie.
2/7