- Pré-requis et Objectifs
-
Cours
-
Contenu
-
1 - Le cadre réglementaire : une multiplication des interventions du législateur suite aux crises sanitaires
- 1.1 - La loi 93-5 du 4 janvier 1993 relative à la sécurité en matière de transfusion sanguine et de médicament
- 1.2 - La loi 98-535 du 1er juillet 1998 relative au renforcement de la veille sanitaire
- 1.3 - Loi 2002-303 du 4 mars 2002 relative aux droits des malades et à la qualité du système de santé
- 1.4 - Loi n° 2004-806 relative à la politique de santé publique du 9 août 2004
- 1.5 - Loi HPST du 21 juillet 2009…et son arsenal de décrets
-
2 - L’organisation du contrôle sanitaire
- 2.1 - Les titulaires du pouvoir de contrôle
-
2.2 - Les agences sanitaires
- 2 . 2 . 1 - L’agence française de sécurité sanitaire des produits de santé ANSM
- 2 . 2 . 2 - La Haute Autorité en Santé (HAS)
- 2 . 2 . 3 - L’institut de veille sanitaire (INVS)
- 2 . 2 . 4 - L’Etablissement Français du Sang (EFS)
- 2 . 2 . 5 - L’Agence de Biomédecine (ABM)
- 2 . 2 . 6 - Agence nationale de sécurité sanitaire de l'alimentation, de l'environnement et du travail (Anses)
-
3 - Les vigilances sanitaires
- 3.1 - Généralités
- 3.2 - Les différentes vigilances
- 3.3 - Le fonctionnement des vigilances
- 3.4 - L’hémovigilance
- 3.5 - La pharmacovigilance
- 3.6 - La materiovigilance
- 3.7 - La réactovigilance
- 3.8 - La biovigilance
- 3.9 - La gestion du risque infectieux : organisation de la lutte contre les infections nosocomiales (IN).liées aux soins
- 3.10 - La cosmetovigilance
- 4 - Les vigilances sanitaires : mode d’emploi
- 5 - Bibliographie
-
1 - Le cadre réglementaire : une multiplication des interventions du législateur suite aux crises sanitaires
- Version Enseignants
-
Version PDF

-
Contenu
- Annexes
- Votre Avis
- Ressources Enseignants
3 - Les vigilances sanitaires
3 . 1 - Généralités
Les vigilances sanitaires représentent une veille sanitaire permanente dont les objectifs sont le signalement, le traitement et l’investigation des évènements indésirables liés à l’utilisation des produits et biens thérapeutiques, la traçabilité de ces produits et la réponse aux alertes sanitaires.
Elles participent à une culture de la sécurité en conduisant chaque professionnel de santé à se poser la question du risque.
Comme tout professionnel de Santé, la sage-femme participe activement à cette prévention des risques et à l’obligation de déclarer les incidents et les dysfonctionnements notamment lors de l’utilisation de matériel
Les vigilances sanitaires ont été instituées par la loi 98-535 du 1er juillet 1998. Elles se sont développées afin de sécuriser les produits de santé en surveillant les évènements indésirables et les incidents. La coordination des déclarations d’évènements est assurée par l'ANSM .
3 . 2 - Les différentes vigilances
Les vigilances correspondent à la surveillance du risque d’effets indésirables ou inattendus, d’incidents ou risque d’incidents résultant de l’utilisation de différentes substances.
Les principales vigilances sont :
- Biovigilance Organes, tissus cellules
- Cosmetovigilance : produits cosmétiques
- Hémovigilanc : Produits sanguins labiles
- Infectiovigilance : infections associées aux soins
- Materiovigilance Dispositif médicaux
- Pharmacovigilance Médicaments et médicaments dérivés du sang
- Réactovigilance : Réactifs de laboratoire
- Toxicovigilance : surveillance des effets toxique de produits, substances ou pollution
Les vigilances relève d'une une mission transversale de tout établissement de santé. Le législateur a rendu obligatoire la déclaration de ces vigilances par l’ensemble des professionnels de santé.
3 . 3 - Le fonctionnement des vigilances
Le fonctionnement des vigilances repose sur 3 piliers :
- L’obligation de déclaration
- Le respect des suivis de l’information
- La participation des acteurs
3 . 3 . 1 - La déclaration
Elle repose sur :
- l’identification de l’évènement et sa mise en relation avec un produit de santé,
- la notification au correspondant chargé du signalement et de son émission.
3 . 3 . 2 - La traçabilité
C’est l’un des éléments incontournables.
La traçabilité permet de retrouver toutes les informations concernant un produit depuis sa fabrication jusqu'à sa destruction.
3 . 3 . 3 - La mobilisation des acteurs
Le système de vigilance repose sur le signalement des évènements indésirables, incidents ou accidents par l’ensemble des professionnels de santé.
Cela nécessite la formation des professionnels et des futurs professionnels à cette culture de la sécurité sanitaire et du signalement.
Les retours d’expérience sur les circuits d’information, les fiches d’évènement indésirables sont primordiaux.
3 . 4 - L’hémovigilance
3 . 4 . 1 - Définitions
Hémovigilance :
« Ensemble des procédures de surveillance organisée depuis la collecte du sang et de ses composants jusqu’au suivi des receveurs en vue de recueillir et d’évaluer les informations sur les effets inattendus ou indésirables résultant de l’utilisation des produits sanguins labiles (PSL), pour en prévenir l’apparition » art R1221.22 du CSP
Elle porte sur l’ensemble de la chaine transfusionnelle allant de la collecte des PSL jusqu’au suivi des receveurs.
Le recueil et l’évaluation des « informations sur les incidents graves ou inattendus survenus chez les donneurs » et le suivi épidémiologique des donneurs relèvent de l’hémovigilance.
Acte transfusionnel : concerne tous les types de produits sanguins labiles homologues ou autologues (CGR, PFC, plaquettes, granulocytes). Il oblige à un contrôle ultime prétransfusionnel, étape indispensable divisée en 2 temps essentiels :
- Le contrôle ultime de concordance entre le patient, les produits et les documents
- Le contrôle ultime de compatibilité du patient et du produit
Il impose une surveillance clinique vigilante du patient.
Sécurité transfusionnelle : ensemble des mesures visant à réduire ou éliminer les risques immunologiques et infectieux liés à la transfusion de produits sanguins. Elle doit être la préoccupation de tous personnels impliqués dans l’acte transfusionnel. La sécurité transfusionnelle repose sur la bonne exécution de chacune des opérations mais aussi sur l’efficacité de leur coordination.
Délivrance des PSL : la mise à disposition de PSL est établie sur prescription médicale en vue de leur administration à un patient déterminé. Elle est effectuée en veillant à la compatibilité immunologique, dans le respect de la prescription médicale et la mise en œuvre des règles d’hémovigilance.
Traçabilité : possibilité, à partir d’une identification enregistrée, de retrouver rapidement l’historique, l’utilisation et la localisation d’un produit sanguin à toute les étapes de sa préparation, ou de sa distribution ou, selon le cas, le(s) receveur(s) au(x)quel(s) il a été administré. La traçabilité d’un PSL désigne l’établissement, le lien entre le donneur, le don, les produits et leur devenir, qu’ils aient été ou non utilisés.
Effet indésirable : réaction nocive survenue chez les donneurs et liée ou susceptible d’être liée au prélèvement ou survenue chez les receveurs et liée ou susceptible d’être liée à l’administration d’un produit sanguin labile.
3 . 4 . 2 - Organisation et missions de l’Hémovigilance
Les missions :
Signalement et déclaration des effets indésirables transfusionnels et des incidents graves de la chaine transfusionnelle
- Traçabilité des produits sanguins labiles
- Conduite d’enquêtes ascendantes et descendantes
- Informations et suivi du patient
- Formation des professionnels de santé
Le comité de la Sécurité transfusionnelle et de l’Hémovigilance (CSTH) :
Il est obligatoire dans chaque établissement de santé
- Veille à la mise en œuvre des règles et procédures d’hémovigilance
- Contribue par ses études et propositions à améliorer la sécurité des patients
- Met en place un programme de formation des professionnels de santé en matière de transfusion sanguine
- Prend des mesures adaptées pour réduire le nombre de PSL détruits
- Fait le bilan annuel des dysfonctionnements graves de la chaine transfusionnelle
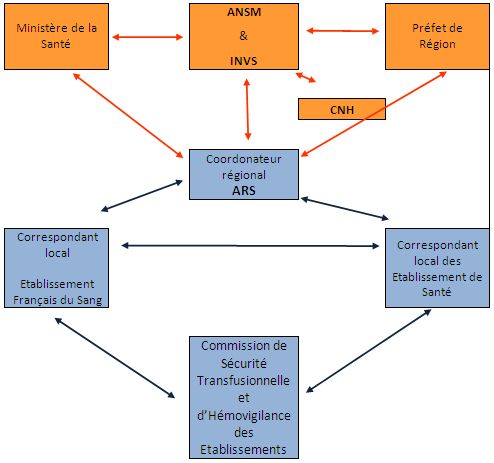
Le parcours de signalement à l’échelon national et régional :
Le tableau ci-dessous présente succinctement les différentes structures agissant aux niveaux national et/ou régional
Figure 2 :
ANSM= agence de sécurité du médicament et des produits de santé
CNH = commission nationale d’Hémovigilance
CSTH = commission de sécurité transfusionnelle et d’Hémovigilance des établissements
ARS = agence régionale de santé
3/6