3.
4 - Ciments verres ionomères
Etant donné que dans la préparation de la poudre pour silicate, on réalise par fusion un verre contenant de la chaux, de l’alumine, du sodium, des fluorures divers et de la silice, Wilson et Kent ont pensé, en 1969, qu’une poudre analogue à celle-ci, susceptible de libérer en milieu acide des ions bi ou trivalents, pouvait interagir avec l’acide polyacrylique, comme ZnO et MgO. Ceci pour obtenir un ciment beaucoup moins opaque que les précédents. Les cations bi et trivalents réagissent sur l’acide polyacrylique et provoquent son durcissement par réticulation.
Les ciments verres ionomères sont des polyacrylates complexes ou polyalkénoates de verre.
Les propriétés sont comparables à celles des ciments polyacryliques. Les ciments à verre ionomère ont été également utilisés comme ciments de scellement en raison de l’adhérence de l’acide polyacrylique sur les tissus dentaires de base.
La force d’adhésion est comparable à celle de certains agents de collage dentinaire. L’adhérence est de 3,8 MPa pour l’émail et de 2,4 pour la dentine. Elle est améliorée par mordançage (acide polyacrylique) 40 % pendant 10 secondes puis rinçage à l’eau). L’adhérence est due aux interactions ioniques dipolaires (COOH) et aux liaisons métalliques plus fortes (Ca). Les CVI entraînent la chélation du calcium. L’adhérence serait mauvaise pour les alliages précieux et les céramiques.
3.
4.
1 - Indications
Les ciments verres ionomères sont utilisés pour :
- le scellement : type 1
- les lésions cervicales et les érosions de classe V ou les bases intermédiaires : type 2
Avec deux catégories :
- a : esthétiques
- b : renforcés (cermets).
- comme fond intermédiaire, dans la technique « sandwich » : type 3
- les fissures : type 4.
3.
4.
2 - Composition
Au départ, les ciments ionomères étaient présentés sous la forme d’un liquide (acide polyacrylique) et d’une poudre (verre ionomère). Par la suite, étant donné la tendance à la polymérisation spontanée de l’acide polyacrylique en solution, on a réalisé des ciments à l’acide polyacrylique anhydre mélangé à la poudre de base. Il suffit de mélanger la poudre avec de l’eau pour solubiliser l’acide polyacrylique. Ces ciments sont improprement appelés ciments polymérisables par l’eau.
La poudre comporte des alumino-silicates fluorés (fluorure de calcium). Le fluor joue sur le pH et le temps de prise.
Composition de la poudre :
- silice SiO2 : 30 %
- alumine Al2O3 : 16 %
- cryolithe Na3AlF : 5 %
- fluorure de calcium CaF2 : 34 %
- trifluorure d’aluminium AlF3 : 5 %
- phosphate d’alumine AlPO4 : 10 %
Le rapport SiO
2/Al
2O
3 est plus élevé que pour les silicates traditionnels.
Le liquide est une solution aqueuse (50 %) copolymère d’acide polyacrylique avec, pour 45 à 50% :
- de l’acide itaconique (durcisseur)
- de l’acide tartrique (accélérateur de la prise)
- de l’acide maléique (durcisseur).
3.
4.
3 - Réaction de prise
Au contact du liquide, la poudre se décompose en surface pour libérer les ions Ca
2+, Al
3+, F
-.
SiO
2 constitue le verre restant.
La poudre et le liquide, mélangés, donnent une masse plastique qui durcit avec le temps. Les cations bivalents et trivalents qui réagissent sur l’acide polyacrylique et provoquent son durcissement par réticulation. La réaction de prise se fait en deux temps :
- les ions Ca2+ se lient aux chaînes de polyacrylate, donnant un gel plastique et sont combinés au bout de trois heures
- les ions Al3+ continuent à réagir pendant 48 heures.
Lors de la prise, il y a :
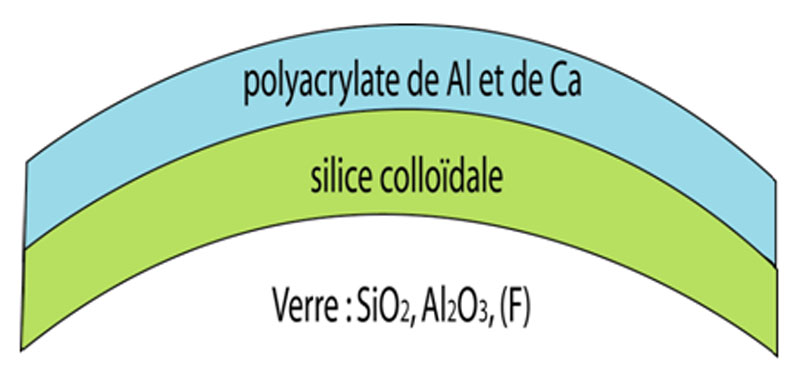
- formation d’un gel de silice hydratée à la surface du verre
- formation de polyacrylate de calcium Ca et d’aluminium Al.
Structure de type matrice à cœur :
- matrice : sel complexe de polyacrylate de calcium et de polyacrylate d’aluminium
- cœur : particules de poudre de verre enrobées dans un gel silicique qui a perdu ses cations.
9/13