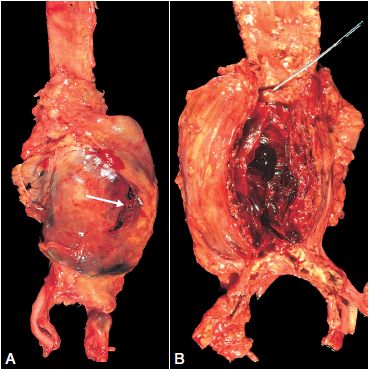
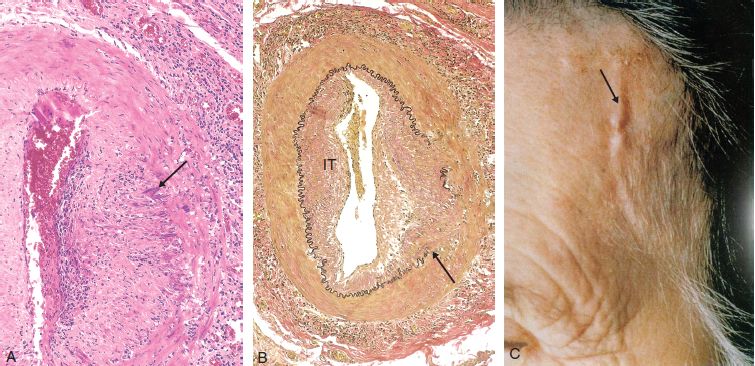
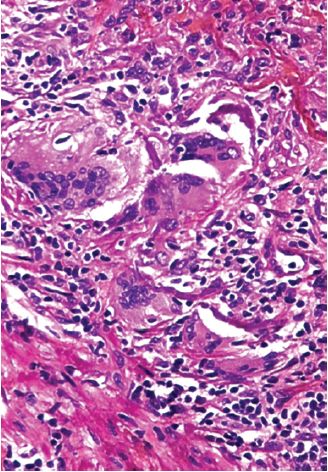
L’hyperlipidémie et les autres facteurs de risque sont supposés entraîner des lésions de l’endothélium, ayant comme conséquence l’adhérence des plaquettes et des monocytes, la libération de facteurs de croissance (en particulier le PGDF), ce qui conduit à la migration et à la prolifération des cellules musculaires lisses. Les cellules spumeuses des plaques athéroscléreuses dérivent à la fois des macrophages et des cellules musculaires lisses : (1) des macrophages par l’intermédiaire des récepteurs des VLDL (lipoprotéines de très basse densité), et des récepteurs éboueurs reconnaissant des LDL (lipoprotéines de basse densité) modifiées (par ex. des LDL oxydées) ; (2) des cellules musculaires lisses grâce à des mécanismes plus mal connus. Les lipides extracellulaires proviennent de la lumière du vaisseau (phénomène d’«insudation»), particulièrement en présence d’une hypercholestérolémie, et aussi de la dégradation de cellules spumeuses. L’accumulation du cholestérol dans la plaque est la conséquence d’un déséquilibre entre ses entrées et ses sorties, et il est possible que les lipoprotéines de haute densité (HDL) puissent aider à éliminer le cholestérol de ces amas. Les cellules musculaires lisses migrent vers l’intima, se multiplient et produisent des constituants de la matrice extra-cellulaire, notamment du collagène et des protéoglycanes.